新陈代谢(metabolism)是生命活动的基本形式。物质代谢包括物质的合成代谢(anabolism)和分解代谢(catabolism)两个过程,一般合成代谢需要消耗能量,而分解代谢产生能量。通过新陈代谢,机体同环境之间不断地进行着物质交换,同时体内物质又不断进行分解、利用与更新,为个体的生存、活动、生长、发育、生殖和维持内环境恒定,提供代谢底物与能量。合成代谢是营养物质进入人体内,参与机体众多的化学反应,在机体内合成较大分子并转化为自身物质的过程,并以糖原(glycogen)、蛋白质(protein)和脂肪(fat)的形式储存在体内,这一反应过程常需要耗能。分解代谢是体内的糖原、蛋白质和脂肪等大分子物质分解为小分子物质的降解过程,常伴有能量的生成与释放。中间代谢(intermediary metabolism)是指营养物质进入机体后,在体内合成、分解、转化和代谢中的一系列化学反应。
【代谢性疾病】
(一)代谢性疾病病因
随着分子生物学技术的迅速发展,近几年来已查明了许多代谢性疾病的病因,这类疾病的共同特点是参与某物质代谢的酶基因或其相关因子存在缺陷,其中以基因的失活性突变为多见,有些代谢性疾病的发病还与调节该种代谢的激素、代谢酶及它们的受体变异有关。有些疾病的致病基因突变类型可多达数十种甚至数百种,并且仍在不断被发现中,但是除代谢障碍的程度差别外,某种代谢障碍的临床表现一般相同或相似,而由此引起的表型则相差悬殊,这给诊断和病情评估带来了极大的困难。
(二)代谢性疾病与内分泌疾病的联系
从分子病因上看,代谢性疾病与内分泌疾病已经没有明确的界限。例如,肥胖是由于脂肪代谢紊乱所致的能量代谢性疾病,但肥胖涉及的病因均与物质代谢的调节激素(如胰岛素、肾上腺素和瘦素等)及其受体功能有关。另一方面,饮食习惯和摄食行为的控制又是一种个体化极强和心理色彩浓厚的主观活动。又如,慢性肾病是继发性甲旁亢的主要病因,但慢性肾病-矿物质骨病(chronic kidney disease-mineral and bone disorders,CKD-MBD)的基本特点是涉及糖类、脂肪、蛋白质、维生素、矿物质及微量元素等多种物质的代谢异常,而这些物质的代谢既受控于相关激素的调节,又随着环境因素的变化而显现出不同的表型差异。物质与能量的代谢性疾病种类很多,范围广泛。人们借助分子生物学技术发现了许多新的代谢性疾病和营养性疾病,如钙受体病、透析性铝中毒骨病(现已少见)和锌缺乏性脑病等。
【能量代谢】
(一)组织和细胞能量代谢
组织和细胞水平的能量代谢(energy metabolism)已经成为近代生物学研究的重点,原因是它与组织损伤和疾病的预后关系更为密切。例如,使用定量分子显像(quantitative molecular imaging)技术(如PET和磁共振光谱法)发现,作为杂食动物的人类心脏,其代谢依赖于个体的代谢适应性(metabolic flexibility);在心肌缺血情况下,代谢适应性是保证心肌胰岛素介导的葡萄糖处理(insulin-mediated glucose disposal)和代谢-机械偶联(metabolicmechanical coupling)的必要前提。当发生肥胖、糖尿病和缺血性心肌病时,心肌对脂肪酸的摄取与氧化增多,并进而发展为能量代谢紊乱和心肌机械收缩功能异常。心衰时,心肌出现代谢中毒(metabolic toxicity),表现为严重的线粒体功能紊乱,脂肪酸失利用和ATP耗竭。其实,代谢适应性障碍和代谢中毒是许多疾病的一种普遍现象,在很多病理情况下,其他组织也出现类似的病理生理改变。
(二)能量代谢与物质代谢的偶联
机体在代谢过程中,需要将体外宏量营养素中的能量转化为机体自身的贮存能量和代谢所需的能量,其转化效率的个体差异很大。这种差异可以理解为代谢效能(metabolic effect)。例如,人类的正常体重事实上反映了人群中脂肪储存的巨大差异,从瘦到胖组成一个连续的体重谱,而胖者和瘦者的Na+-K+-ATP酶活性和对各种激素及环境刺激的代谢效能相差悬殊,这种差异主要由个体的基因组特性决定,其中瘦素和β3-肾上腺能受体基因的表达差异在肥胖的形成中有重要作用,故认为它们是肥胖的候选基因。
1.能量消耗
机体的能量消耗(energy consumption)包括静息代谢率(resting metabolic rate,RMR)、运动性生热效应(thermic effect of exercise,TEE)、食物性生热效应(thermic effect of food,TEF)及兼性生热作用(facultative thermogenesis,FTM)。RMR的个体差异主要由机体的非脂肪体质(fat-free mass)及其遗传差异决定。此外,能量消耗也受甲状腺激素水平和交感神经活动强度等的影响。TEE主要由活动强度决定,其个体差异不明显。而TEF主要用于营养素同化过程(assimilation process)的能量消耗,约占每天能量消耗的10%。FTM由环境、温度、进食和情绪变化等因素引起,在寒冷环境中,机体的产热主要来源于棕色脂肪的分解。棕色脂肪细胞(brown adipocyte)和肌细胞的胚胎来源相同,而与白色脂肪细胞的胚胎来源不同。棕色脂肪细胞与白色脂肪细胞可以在特定条件下相互转化(转分化,转型分化,transdifferentiation),但在转型分化过程中也产生米色(brite)脂肪细胞,提示脂肪细胞具有很大的分化可塑性(plasticity)。寒冷环境诱导热能生成,葡萄糖利用率增加10~15倍,用PET可以清楚地观察到棕色脂肪组织的代谢变化。为了维持体重稳定,能量的供给和消耗必须是平衡的。能量消耗主要包括基础状态耗能和体力活动耗能两部分。
每日所需能量为基础能量消耗、特殊功能活动和体力活动等所消耗能量的总和。基础能量消耗可因性别、年龄、身高和体重的不同而异,临床可按Harris-Benedict公式推算。特殊功能活动除包括消化和吸收所消耗的能量外,还可因生理特殊需要如生长、发育、妊娠和哺乳等情况而增加。体力活动所需的能量因强度的不同而异,轻、中、重体力活动所需能量分别为基础能量的30%、50%、100%或更多。专业运动员的骨骼肌能量转换要比正常人高20~100倍。在某些情况下,能量代谢紊乱将导致肥胖或消瘦,并进而引起一系列代谢异常、器官功能障碍和组织损害。在物质供应和获得充分的条件下,可能仅仅因为生活习惯与方式的异常而导致能量过剩(肥胖)及其众多并发症。
2.节俭基因型与代谢综合征
人类进化过程中所选择的“节俭基因型”有利于食物充足时促进脂肪堆积和能量储存。进食后能较多地将食物能量以脂肪形式储存起来的个体较易耐受长期饥饿。但是,“节俭基因型”个体在食物充足条件下转变成肥胖易感基因,这些个体易出现代谢综合征(肥胖、胰岛素抵抗、高血压和糖尿病等)。
3.运动对器官功能的影响
长期以来认为,当机体的某一器官或组织出现较严重病变时,需要强调制动和休息,以确保病变康复。研究发现,对于早期甚至中期的器官病变来说,这种观点并无充足的根据。与以前的看法不同的是,有规律的长期锻炼和运动(尤其是耐力运动训练,endurance exercise training)是保护心肌免受损害和增强免疫功能的一种有效途径。体育运动获益可以发生在机体的不同层面(一般以线粒体水平为主),而心脏保护(cardioprotection)的机制未明,可能主要与线粒体的氧化-还原反应改变(redox change)有关。一个显而易见的事实是,运动能使线粒体的伴侣蛋白(mitochondrial chaperone)表达上调,抗氧化能力增强,对抗细胞死亡的保护分子浓度升高,并能降低肝内脂肪沉积。在某些情况下,运动还能降低线粒体膜的通透性和线粒体中毒(mitotoxicity)的易感性。研究还发现,以每周代谢当量小时(metabolic equivalent hours of per week)计算,体力活动,尤其是较高强度的体力活动可以延长癌症患者的存活期,虽然这对于晚期肿瘤患者来说很难做到或者根本无法做到,但这些观察提示,通过体力活动增强机体的代谢水平对于疾病的防治是何等重要。
4.食物摄入对能量代谢的作用
食物进入胃肠道,在消化液、酶和激素等作用下转变为单糖、氨基酸、短链-中链脂肪酸、甘油、水、矿物质和维生素等,一起被吸收入血,中性脂肪酸和多数长链脂肪酸则经淋巴系统入血,在肝和周围组织中被利用,以合成机体自身物质或分解供能。机体的自身物质亦随时分解,提供能量或合成新的物质。糖、蛋白质、脂肪、水和无机元素的代谢反应受基因调控,并通过酶和神经-内分泌系统进行精细调节。代谢底物的质和量,辅因子、体液组成和离子浓度等反应环境,中间和最终产物的质和量等,都对中间代谢的调节起重要作用。中间代谢所产生的物质除被机体储存或重新利用外,最后以水、二氧化碳、含氮物质或其他代谢终产物形式,经肺、肾、肠和皮肤黏膜等排出体外。
在现代社会里,人们的营养物质分配与消耗很不合理,在营养缺乏性(nutrition-deficiency)疾病仍然盛行的同时,出现了营养过剩相关疾病的流行,代谢综合征与其相关性疾病的大流行成为现代社会疾病谱的突出特点。在我国,随着人均寿命的延长和社会与经济的进步,原发性营养缺乏性疾病已经少见;而由于血液透析、静脉营养支持、器官移植和癌症化疗等的普遍应用,伴发的继发性营养障碍性疾病(nutrition disturbance disease)越来越多见,必须引起高度重视。地域性食物习惯与饮食摄入是许多疾病的重要环境因素。例如,有些肿瘤的发病率具有明显的地域流行特点,当人们从低发病率的地区移居到高发病率地区后,这些人群发生某种肿瘤的概率急剧增高。这说明,地理环境对肿瘤(如乳腺癌和结肠直肠癌)的发生有明显影响。在众多的环境因素中,最受关注的是营养因素、能量平衡(energy balance)、代谢状态(metabolic status)与调节代谢的相关激素等。因此,这些肿瘤是可以通过改变营养、代谢和相关激素水平而达到预防目的的。
5.代谢记忆效应
组蛋白(histone)被翻译后修饰(posttranslational modification,PTM)分子所包裹。Gardner等提出表观遗传学(epigenetics)假说,认为PTM是管理和调节核染色质功能的关键分子(组蛋白密码,histone code),开创了非基因序列改变和组蛋白的表观修饰与功能组蛋白的修饰与功能、染色质重塑、结构与功能以及基因组印记等方面的研究。目前看来,代谢记忆可以引起组蛋白密码的变化,控制饮食能影响表观遗传学相关信息的表达。因此,基因与环境的关系可以导致染色质的特异性变化,而早期强化治疗控制糖尿病高血糖可出现良好的代谢记忆效应(good metabolic memory effect)的观点已经被反复验证。
心血管事件是导致糖尿病肾衰患者死亡的主要危险因素,虽然高LDL-胆固醇血症和高C-反应蛋白症起了一定作用,但降低这些危险指标后,患者的预后并无明显改善,这是长期氧化应激记忆效应的结果。氧化应激造成糖化终末产物(AGE)堆积,后者与AGE受体(RAGE)作用,产生细胞内氧化应激炎性介质,进一步扩增氧化应激效应。因此,AGE/RAGE在心血管事件的发生和发展中起了不良代谢记忆效应(bad metabolic memory effect)。
6.饮食治疗
饮食治疗是肥胖和代谢综合征的另一种重要手段。从生活质量方面考虑,除了限制热能供应外,如何增加饱感已经成为重要的研究课题。饱感(satiety)受食物的量和组成成分的影响。人们发现,食物中的水分和气体含量具有较强的刺激饱感和抑制食欲作用,因而后者也成为控制体重的时髦方法之一。饮食治疗也是其他许多代谢性疾病的处置方法之一。例如,除经典的苯丙氨酸限制饮食治疗苯丙酮尿症(phenylketonuria)外,使用的大分子中性氨基酸(large neutral amino acid,LNAA)补充治疗可以明显降低血液与脑组织的苯丙氨酸浓度,改善患者的认知功能和生活质量;又如,补充氨基酸(尤其是亮氨酸)可改善肌肉重建(muscle remodeling)功能,防止肌肉萎缩。肌肽(carnosine)和β-丙氨酸(beta-alanine)是运动时能量代谢的关键物质,补充肌肽和β-丙氨酸可能增加其在肌肉中的含量,提高肌肉对pH的调节能力和肌肉耐力。
【物质代谢】
(一)必需营养素
人体所需要的营养物质按其化学特性和生理功能可归纳为六类(表1),包括碳水化合物(carbohydrate)、脂肪、蛋白质、维生素(vitamin)、矿物质(mineral)和水(water),其中一些必须由外界供给(如绝大多数维生素,主要来自食物),另一些则可在体内合成。必需营养素(essential nutrient)是指体内不能生成的营养成分,每日膳食供给量系指正常情况下,能维持机体正常身高和体重、组织结构与生理功能的最少量。
表1 人体所需的营养素

宏量元素(macronutrient)在体内含量较多,如钙、镁、钠、氯和磷等;宏量营养素是可以互相转换的能源,脂肪产热37.7kJ/g(9kcal/g),糖类和蛋白质产热16.7kJ/g(4kcal/g),乙醇产热29.3kJ/g(7kcal/g)。微量营养素(micronutrient)包括维生素及某些无机元素(微量元素),为维持人体健康所必需,一般消耗甚微,不经变化即可被吸收。许多微量元素还有代谢催化作用。微量元素(microelement)在体内含量极少,故又称痕量元素(traced element)。人体内可测得60种以上微量元素,其中11种是被公认的,并有特殊的生理功能,为人体所必需,故又被称为必需微量元素(essential microelement),这些物质主要包括铁、氟、锌、铜、钒、锰、碘、钼、铬、钴和硅,如摄入不足可引起疾病。此外,锂已用于临床治疗精神病和糖尿病,亦可能是具有特殊功能的必需微量元素。锡与镍在人体含量与钒、硒、锰和钼差不多,均分布于皮肤;虽有人将锡与镍纳入必需微量元素,但对其生理作用知之甚少。
(二)蛋白质生物效价和不饱和脂肪酸比例
人体摄入的蛋白质的量与质是营养学上一个十分重要的研究课题,也是衡量食物质量的重要指标。1965年,联合国粮食及农业组织(FAO)推荐的成人每日氮(N)的基础排泄量(最低代谢需要量)为50mgN/kg,但维持氮的总平衡(total balance of nitrogen)的最低氮摄入量约为75mgN/kg。目前被公认的成人优良蛋白质摄入的推荐供给量(RDA)为95~125mgN/kg,相当于600~800mg蛋白质/kg。但是,多数人在蛋白质的实际消耗方面,可能远远超过以上的推荐供给量。这就意味着,如果没有必要将蛋白质作为主要的能量物质来对待的话,那么这种浪费无形中增加了机体的代谢负担,这对于老年人群和肾脏功能不全者来说,未必是健康的。
许多情况下,蛋白质的“质量”可以通过食物互补和食物混合来提高,以增加必需氨基酸(essential amino acid)的含量,优化其比例。生物效价为80以上的蛋白质,成人每千克理想体重约需1g/d。蛋白质生物效价的顺序依次为:动物制品>豆类>谷类(米、小麦>玉米),例如,牛奶与鸡蛋的蛋白质生物效价为93,牛肉为76,麦片和大米为65,玉米为50。如供应的蛋白质的生物效价较低,则每日的所需量应适当增加。脂肪所供应的能量不宜超过总能量的30%。每日所需的总能量除由蛋白质和脂肪供应外,余下的主要由碳水化合物供应。在供应的脂肪中,饱和脂肪酸、多价不饱和脂肪酸与单价不饱和脂肪酸的比例应为1∶1∶1,每日的胆固醇摄入量宜在300mg以下。
(三)细胞酶缺陷或膜转运异常
代谢酶的功能或结构缺陷可使代谢途径的流向改变和/或合成途径的反馈调节紊乱,导致代谢产物缺失或过多,中间产物堆积,或转变为毒性代谢物,产生相应的病理改变和临床表现。例如,半乳糖血症是由于第17、9或1号染色体上基因异常,在半乳糖转变为葡萄糖过程中,缺乏半乳糖激酶或半乳糖-1-磷酸尿苷酰转移酶或尿核苷二磷酸-4-异构酶,导致血液、尿液和组织中的半乳糖及其代谢产物水平升高,并有白内障、肝硬化、肾小管功能异常和智能障碍等临床表现。膜转运异常多为特定功能的膜载体蛋白缺陷所致,例如胱氨酸尿症、肾性糖尿和家族性高胆固醇血症等。先天性代谢缺陷和环境因素在代谢病的发病中起着不同作用,但又关系密切。先天性代谢缺陷为发病的基础,而环境因素常为发病的诱因。例如,苯丙酮尿症是由于苯丙氨酸羟化酶缺乏引起,食物中如富含苯丙氨酸可导致高苯丙氨酸血症,使特异组织或器官受损,出现功能障碍。但如在出生后3周内确诊,限制苯丙氨酸的摄入量,可防止本病的发生与发展。除酶的结构外,细胞内底物的亲和性(substrate affinity)和负性选择(negative selection)也决定了代谢酶的特异性。机体细胞的调节系统能尽量减少酶与其他无关物质的相互作用,但是,在细胞内的核酸代谢过程中,许多药物或外来物质可以作用于酶促反应,干扰正常的核酸代谢,或起到治疗作用,或产生细胞毒性。最近用结构性基因组聚生体(structural genomics consortium,SGC)技术发现了数十个核酸代谢的酶结构域,它们可能成为核酸代谢的干预靶点。
(四)物质代谢异常
1.蛋白质营养障碍与蛋白质代谢障碍
蛋白质营养障碍主要包括:①蛋白质和氨基酸不足:如蛋白质-能量营养不良、蛋白质缺乏症、赖氨酸缺乏症和营养相关性肿瘤;②氨基酸过多:如酪氨酸和蛋氨酸在肝功能失代偿期可诱发肝性脑病。此种情况一般只在原有器官疾病的基础上发生。蛋白质代谢障碍主要包括:①继发于器官疾病:如严重肝病时的低蛋白血症,淀粉样变的免疫球蛋白代谢障碍;②先天性代谢缺陷:引起蛋白质合成、降解或转运异常,如白化病、各型血红蛋白病和无纤维蛋白血症等。
2.碳水化合物代谢异常
主要有:①碳水化合物摄取过多:引起肥胖症和糖尿病;②碳水化合物摄取不足:伴有能量不足时常致消瘦;③各种原因所致的低血糖症;④先天性酶系缺陷所致的糖代谢异常,如果糖不耐受症、半乳糖血症和糖原贮积症等。
3.脂类代谢障碍
主要有:①脂类摄取过多:引起肥胖症和血脂异常症,以血浆胆固醇和/或甘油三酯浓度升高为标志,可为先天性代谢紊乱,亦可继发于其他疾病。前者有家族性高胆固醇血症、异常β脂蛋白血症、家族性高甘油三酯血症等;②脂类摄取过少:常引起脂溶性维生素缺乏症。
4.核酸代谢障碍
在核酸和核苷酸的正常转换过程中,部分被降解成游离嘌呤基,主要是次黄嘌呤和鸟嘌呤。合成核酸所需要的核苷酸过剩时,会迅速降解为次黄嘌呤。鸟嘌呤在鸟嘌呤酶作用下脱氨成为黄嘌呤。次黄嘌呤和黄嘌呤经黄嘌呤氧化酶作用被氧化成尿酸。腺嘌呤核苷酸、次黄嘌呤核苷酸和鸟嘌呤核苷酸是嘌呤生物合成的末端产物。上述3种嘌呤核苷酸可经两条途径中的一条直接从嘌呤碱合成,如鸟嘌呤转化成鸟嘌呤核苷酸;次黄嘌呤转化成次黄嘌呤核苷酸;腺嘌呤转化成腺嘌呤核苷酸。或者,它们可重新合成。嘌呤代谢的首步反应及其反馈抑制的部分是磷酸核糖焦磷酸(PRPP)+谷氨酰胺+H2O氨基磷酸核糖+谷氨酸+焦磷酸(PPI),该反应由磷酸核糖焦磷酸酰胺转移酶(PRPPAT)催化。
大多数原发性高尿酸血症的病因未明,少数可由于酶的缺陷引起。发病与尿酸生成过多或肾尿酸排泄减少有关。在有痛风史的家庭中,无症状高尿酸血症者占25%~27%。Hange和Harvald研究了32例痛风患者的261个亲属,6.1%有痛风。另两项关于痛风家族的研究显示,25%有高尿酸血症,而正常人群仅4.6%。多数学者认为,高尿酸血症的分布方式与多基因遗传有关,同时在饮食和其他环境因素的作用下而发病。许多系统性疾病因核酸分解代谢亢进、摄入过多和尿酸排泄被抑制而引起继发性高尿酸血症,如溶血性贫血、肿瘤、红细胞增多症、系统性红斑狼疮、慢性肾小球肾炎、肾盂肾炎、多囊肾、铅中毒、高血压晚期、糖尿病酮症酸中毒、乳酸性酸中毒及酒精性酮症、肝肾移植、化疗、放疗、灼伤、挫伤或药物等。高尿酸血症与肥胖的关系密切,胰岛素抵抗及内脏脂肪型肥胖等多危险因子综合征(multiple risk factor syndrome)与高尿酸血症有关,同时与动脉硬化性疾病的发生和发展关联。
5.水与电解质代谢异常
多为获得性,亦可见于先天性缺陷,如先天性肾上腺皮质增生症。水和电解质营养障碍引起水和电解质代谢平衡紊乱,如尿崩症、水中毒、失水、高(低)钠血症、高(低)钾血症、高(低)钙血症、高(低)镁血症和高(低)磷血症等。
6.无机元素代谢异常
如铜代谢异常所致的肝豆状核变性,铁代谢异常所致的含铁血黄素沉着症等。碘是生物体内必需的微量元素之一,而甲状腺是唯一能浓聚和利用碘的内分泌腺体。但是,乳汁中的碘含量与母亲的饮食碘量相关,差异甚大;而婴幼儿的甲状腺储存量很低,因而其对乳汁中的碘含量很敏感。全世界约有8亿人口生活在缺碘地区,约2亿人患有与碘缺乏相关的甲状腺肿。经过近半个世纪的补碘防治,目前在一些发达地区已基本控制了碘缺乏病的流行,但缺碘仍然是本世纪的重大社会和卫生健康问题。同样,低锌状态也较普遍,老年人常发肺部感染可能与缺锌有关。无机元素营养障碍表现为微量元素不足或过多。在临床上,以微量元素缺乏较多见,尤其多见于儿童、孕妇和已有营养不良者。
7.维生素代谢异常
维生素类可分为脂溶性(维生素A、D、E和K)和水溶性(维生素B族和维生素C)两类,维生素营养障碍主要包括各种维生素缺乏症和维生素过多症。传统的观点认为,维生素D缺乏引起骨代谢障碍和佝偻病/骨质软化症,但严重而长期的维生素D代谢紊乱还可导致肌肉和神经功能紊乱,甚至与糖尿病、肿瘤、自身免疫疾病和性腺功能障碍均有关。流行病学调查发现,营养不良性佝偻病/骨软化症仍然是一个世界性的公共卫生问题,维生素D缺乏相当普遍;而长期的维生素D不足与原发性骨质疏松的关系已经得到肯定。维生素B12缺乏的情况也不容乐观,而且与前列腺癌相关。
8.复合型营养障碍
表现为多种营养素障碍的不同组合。完全性非经肠营养(complete parenteral nutrition)液体含有丰富的混合氨基酸,可以提供9种必需氨基酸和其他非必需氨基酸。因而是治疗复合型营养障碍的较佳选择。但是,完全性非经肠营养液体中的谷氨酰胺(glutamine)、精氨酸、支链氨基酸(branched chain amino acid)、半胱氨酸和牛磺酸(taurine)必须控制在适合范围内,否则将引起新的营养障碍。
9.其他代谢异常
如嘌呤代谢障碍所致的痛风,卟啉代谢障碍所致的血卟啉病。
(五)营养失调
营养性疾病(nutritional disease)是指营养素(nutrient)缺乏、不足、过剩或作用障碍等引起的一类疾病。但在临床上,一般意义上的营养性疾病仅指维生素或蛋白质/氨基酸缺乏所致的营养不良或维生素缺乏/不足,并不包括糖类、脂类、无机元素、水和电解质的代谢紊乱在内。营养性疾病和代谢性疾病的关系密切,难以截然分开,该两类疾病往往相互依存,相互影响。例如,维生素D缺乏症常表现为钙磷代谢失常;糖尿病常伴有蛋白质-能量营养不良症(protein-energy malnutrition,PEM)。机体对各种营养物质均有一定的需要量、允许量和耐受量,因此营养性疾病可因一种或多种营养物质不足、过多或比例异常引起。营养性疾病的病因和发病机制多较清楚。
1.原发性营养失调
由于摄取营养物质不足、过多或比例不当所致,与器质性或功能性疾病无关。例如,摄取蛋白质不足引起蛋白质-能量营养不良,而摄取能量超过机体消耗则可导致肥胖症。营养障碍性疾病并不是营养供给缺乏所致,而主要是缺乏对这类疾病的预防意识引起的。营养缺乏性疾病常见,即使在发达国家和地区也不例外。1973年的报告指出,加拿大居民的铁、维生素D、钙、叶酸和维生素A,甚至氟化物的摄入量都较低,而22年后的调查结果并未见明显改善,这些营养素的摄入不足主要发生于儿童人群中,约50%的儿童曾有过铁缺乏;营养不良性佝偻病在某些地区仍很常见。亚临床型维生素A缺乏亦不少见。
2.继发性营养失调
继发性营养失调与营养物质的供给无直接联系,而主要与下列因素有关:①进食障碍:口咽和食管疾病所致的摄食困难,神经性厌食所致的摄食过少。②消化吸收障碍:见于消化道疾病,转运维生素的蛋白质先天性缺乏,一些药物如新霉素、考来烯胺(colestyramine)和双胍类降糖药等均可引起营养素的消化和吸收障碍。③合成障碍:肝硬化失代偿期,由于白蛋白合成障碍引起的低白蛋白血症。甲状腺球蛋白合成障碍引起甲减等。④消耗增多:机体对营养需求的改变如发热、甲亢、恶性肿瘤、慢性消耗性疾病、手术后以及一些生理性因素如生长发育和妊娠等,机体需要的营养素增加,如供应不足可致营养缺乏症。⑤排泄失常:多尿可致失水,腹泻可致机体缺钾,长期大量蛋白尿可致低蛋白血症等。长期血液透析者(尤其是老年患者)可出现一系列营养障碍性疾病。对老年人来说,出现血浆尿素、肌酐、白蛋白和阴离子间隙(AG)明显增加是预后不良(蛋白营养不良症)的表现。慢性透析患者还可能出现Mg、Cu、Zn、Sr、Ba和Pb等的排泌异常。⑥代谢障碍:营养素在体内代谢的任何环节异常均会引起营养素的代谢障碍,其中绝大多数是因为代谢所需的酶缺陷所致,少部分与器官或组织的功能障碍有关。例如,糖原贮积症(glycogen storage disease,GSD)是由于糖原合成和分解所需酶(己糖激酶、磷酸葡萄糖变位酶、糖原合成酶和分支酶等)的先天性缺陷引起的一类遗传性疾病,因糖原合成和分解涉及许多酶,所以不同酶缺陷引起不同类型疾病。不同类型的糖原贮积症虽各有其临床特征,但低血糖症和/或肌无力是所有类型共有的临床表现。又如,特殊类型糖尿病主要有胰岛β细胞功能基因突变所致的糖尿病和线粒体母系遗传性糖尿病与其他特异型糖尿病,青年发病的成年型糖尿病(maturity-onset diabetes of the young,MODY)的病因为糖代谢酶或相关因子突变,现已经查明7种突变基因,即肝细胞核因子(hepatocyte nuclear factor,HNF)4α基因突变(MODY1)、葡萄糖激酶(glucokinase,GCK)基因突变(MODY2)、HNF-1α基因突变(MODY3)、胰岛素增强子因子1(insulin promoter factor-1,IPF-1)基因突变(MODY4)、HNF-1α基因突变(MODY5)、NeuroD1基因突变(MODY6)或胰岛素基因突变(MODYX)。
3.肝病导致的营养障碍
肝脏是机体物质代谢的主要场所,大部分激素的摄取、转变、灭活、降解及排泄等都在肝脏进行。此外,肝脏尚可通过合成部分激素以及某些代谢所需的生物酶和辅助因子而影响机体的其他代谢。因此,肝脏疾病(如肝硬化)可导致营养性疾病。中间代谢受很多因素调控,在导致中间代谢某个环节障碍的诸因素中,大约可分为先天性代谢缺陷和环境因素两类。在内分泌代谢领域内,代谢性疾病的发展十分迅速,尤其是糖尿病和代谢性肝病。例如,肝脏能合成25-(OH)D,此合成过程受肝内和血浆中维生素D及25-(OH)D的控制,而不受钙和磷代谢改变的影响,25-(OH)D的形成即使在大量摄入维生素D期间仍继续生成和蓄积。但在原发性胆汁性肝硬化、自身免疫性肝炎、慢性实质性或胆汁淤积性肝病时,肠道吸收的维生素D不能或极少转化成25-(OH)D,从而导致活化的维生素D减少,使钙平衡紊乱,长期的负钙平衡可导致骨质软化、骨质疏松或佝偻病。
4.器官疾病引起的营养障碍
器官功能障碍的另一个常见原因是衰老。老年人常伴有许多变形蛋白质积蓄(aberrant proteostasis)和线粒体功能障碍,并进而导致能量代谢(energy metabolism)失衡,组织功能紊乱和结构的破坏。
【代谢性疾病的临床特点】
代谢性疾病的临床特点有:①详细的查询病史可发现或提示这类疾病;②发病多与营养素的供应情况、饮食习惯、生活条件与环境因素、消化功能、生理或病理附加因素等有关;③常有家族史和环境诱发因素以及发病年龄和性别等特点,如原发性痛风主要见于男性,苯丙酮尿症在新生儿即可检出;④早期常先有生化和生理改变,以后再出现病理解剖改变,早期治疗病变多可逆转。长期的代谢异常影响个体的生长、发育、成熟和衰老等过程,甚至通过表观遗传方式影响下一代。这些疾病有很多,如家族性原发性甲旁亢、肾上腺皮质功能减退症伴甲旁减、浅表念珠菌病、常染色体隐性家族性甲旁减、甲旁减伴神经性耳聋和肾发育不全、Carney复合症、地塞米松敏感的醛固酮增多症、醛固酮缺乏症Ⅱ型、假性醛固酮不足症、脑硬化、常染色体新生儿型肾上腺白质营养不良、过氧化质体酰基辅酶A氧化酶缺陷症、家族性肾上腺皮质功能减退、遗传型盐皮质激素高血压和Liddle综合征,等等。
代谢性疾病的病因治疗主要针对代谢障碍的环节进行,其中特别重要的是补充或纠正所缺陷的代谢催化酶。最近几年,发展出了一种代谢基因组路径技术(metagenomicapproach),即应用这种技术从环境中收集DNA,以不依赖于DNA序列同源性(sequence homology)方式,通过高通量筛选,寻找或生产新的代谢酶。
【肥胖与糖尿病的基因组代谢】
系统生物学应用人类基因组代谢模型(human genomescale metabolic model,GEM)研究细胞代谢,探讨代谢性疾病的发病机制、生物标志物和治疗药物。GEM最早用于微生物的代谢研究,后来用于线粒体的代谢网络、肥胖和2型糖尿病的病因与发病机制研究。GEM研究发现能量代谢率与众多相关基因的表达改变有关。
在整体水平上,代谢率(metabolic rate)是指O2消耗率(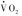 ),包括了线粒体呼吸链的
),包括了线粒体呼吸链的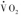 和各种组织的其他氧消耗(图1)。
和各种组织的其他氧消耗(图1)。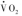 可用于确定ATP转换率,并通过底物氧化途径计算出通量率(flux rate)。但是,测得的呼吸测量并非生理(无氧代谢)状态,影响因素(如体重、体表面积等)多。ATP转换率(ATP turnover rate)或代谢率可代表组织或器官的线粒体呼吸率(mitochondrial respiration rate),其测定需要高技术水平。一种方法是测量运动时的最大有氧代谢率(maximum aerobic metabolic rate,
可用于确定ATP转换率,并通过底物氧化途径计算出通量率(flux rate)。但是,测得的呼吸测量并非生理(无氧代谢)状态,影响因素(如体重、体表面积等)多。ATP转换率(ATP turnover rate)或代谢率可代表组织或器官的线粒体呼吸率(mitochondrial respiration rate),其测定需要高技术水平。一种方法是测量运动时的最大有氧代谢率(maximum aerobic metabolic rate,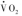 ),此时的运动肌肉占耗氧量和二氧化碳生成量(
),此时的运动肌肉占耗氧量和二氧化碳生成量(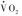 ,rate of carbon dioxide production)的90%,线粒体质子漏(mitochondrial proton leak)最低。能量代谢受多水平多因素调节。在基础状态下,基础代谢率(basal metabolic rate,BMR)维持生物合成和物质转运功能,O2和CO2与物质氧化率低;在高强度运动时,肌肉运动所需的O2消耗和CO2生成率明显增加。最高代谢率(maximal metabolic rate,MMR或
,rate of carbon dioxide production)的90%,线粒体质子漏(mitochondrial proton leak)最低。能量代谢受多水平多因素调节。在基础状态下,基础代谢率(basal metabolic rate,BMR)维持生物合成和物质转运功能,O2和CO2与物质氧化率低;在高强度运动时,肌肉运动所需的O2消耗和CO2生成率明显增加。最高代谢率(maximal metabolic rate,MMR或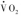 )代表ATP利用和能量物质氧化的最大值。
)代表ATP利用和能量物质氧化的最大值。
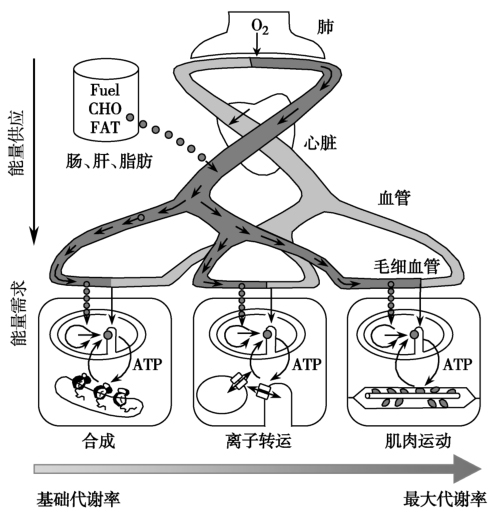
图1 能量代谢的多水平调节
【产能物质代谢病】
(一)碳水化合物代谢病
碳水化合物代谢性疾病的种类众多,糖尿病是其典型代表。除糖尿病外,其他碳水化合物代谢性疾病有继发性糖尿病、遗传性胰岛素不敏感综合征、低血糖症、肥胖症、代谢综合征、糖原贮积症、半乳糖血症、黏多糖贮积症、果糖不耐受和碳水化合物中间代谢缺陷综合征等。
1.糖尿病
糖尿病是由遗传和环境因素共同引起的一组以糖代谢紊乱为主要表现的临床综合征。胰岛素缺乏和胰岛素作用障碍单独或同时引起碳水化合物、脂肪、蛋白质、水和电解质等的代谢紊乱。临床以慢性高血糖为主要特征,其急性并发症有糖尿病酮症酸中毒、高渗性高血糖状态和乳酸性酸中毒。糖尿病可并发多种慢性并发症,导致器官功能障碍和衰竭,甚至致残或致死。全世界的糖尿病患病率迅速增加,发展中国家尤为明显,糖尿病已经成为临床上的主要内分泌代谢病。除少数继发性糖尿病、部分妊娠糖尿病及1型/2型早期糖尿病外,本病一般为终生性疾病,任何病因学类型的糖尿病通常要经过几个临床阶段(高血糖前期、高血糖期和慢性并发期),每个患者可按顺序从一个阶段进入另外一个阶段,但在某些阶段也可逆转。因此,糖尿病治疗的目的是长期全面地控制高血糖和其他代谢紊乱,如高血压、高血脂、肥胖和高凝状态等,保护胰岛β细胞功能,防止和延缓并发症的发生。
糖尿病的治疗必须是长期的和综合性的。但是,特殊患者群应执行灵活的个体化治疗方案,权衡治疗获益(benefit)和治疗风险(risk),治疗方案应该是有效的和可行的。根据中华医学会内分泌学分会糖尿病组提出的建议,无糖尿病并发症和严重伴发疾病的非老年(<65岁)患者一般将HbA1c控制于<6.5%;年轻、病程短、治疗后无低血糖和体重增加等不良反应或单用生活方式治疗者HbA1c<6%;口服药不达标加用或改用胰岛素者HbA1c<7%;伴有心血管病(cvd)或cvd极高危患者的hba1c≤7.5%。老年(≥65岁)和预期生存期>15年者HbA1c≤7%;合并其他疾病,预期生存期5~15年者HbA1c<8%;特殊情况甚至放宽至HbA1c<9%。低血糖高危人群HbA1c不应超过9%。糖尿病患者计划妊娠时HbA1c<6.5%,用胰岛素治疗者HbA1c<7%才宜妊娠;妊娠期间HbA1c<6%。餐前、睡前及夜间的毛细血管血糖不超过5.4mmol/L,餐后峰值不超过7.1mmol/L。妊娠糖尿病餐前5.0~5.5mmol/L,餐后1小时<7.8mmol/L或2小时<6.7~7.1mmol/L。血糖控制必须安全、可行、科学,坚持个体化原则。同时,血糖之外其他心血管危险因素的控制也十分重要。内外科重症监护患者的血糖控制目标为7.8~10mmol/L,一般不必将血糖降至6.1mmol/L以下。非危重住院患者(接受胰岛素治疗者)推荐的餐前血糖为7.8mmol/L,随机血糖为10mmol/L以下。
2.肥胖和代谢综合征
许多资料发现,代谢综合征及其组分(2型糖尿病、中心性肥胖、高血压、高甘油三酯血症、高胆固醇血症、低高密度胆固醇血症和痛风等)加速增龄性认知功能下降、血管性痴呆和老年性痴呆的发展,这种情况可称为代谢-认知综合征(metabolic-cognitive syndrome)。代谢综合征与认知功能障碍的联系因子很多,其中β-淀粉样肽(β-amyloid peptide)代谢异常和tau蛋白的高磷酸化状态可能起了关键作用。
免疫代谢病学(immunometabolism)是专门研究免疫与代谢的相互关系及其对疾病影响的一门新兴学科,研究的主要层面在组织病理学上两者的联系。例如,肥胖的突出病理生理改变是慢性低度炎症,并进而引起一系列的肥胖并发症,在病变的进展过程中,慢性炎症和免疫系统起了重要作用,研究其发生机制,对肥胖相关性疾病的预防与治疗有至关重要的意义。肥胖的治疗必须是综合性的,首先要重视生活方式与摄食行为干预,增加体力活动和能量消耗,体能训练还可以改善心血管功能,提高运动耐量。运动与饮食治疗相结合,体重减轻更明显;如果可能,用极低热量饮食再加上活动可达到更佳效果。
药物仅起到辅助作用,依赖减肥药物的做法是不妥的。西布曲明抑制食欲并增加产热,但可增加心血管事件风险。因而,美国FDA建议对西布曲明的说明书提出黑框警告(black box warning),我国亦于2010年宣布西布曲明退市。奥利司特抑制脂肪吸收,与低脂饮食配合,体重减轻更多。不良反应主要是由于脂肪吸收不良所引起,有稀便、便急和影响脂溶性维生素的吸收。其他药物,如二甲双胍、二硝基酚(dinitrophenol)、甲状腺粉片、麻黄碱和黄嘌呤等有一定的减肥作用,但不良反应多,长期治疗的最终收益未明。肥胖者常通过增加运动量和减少饮食来减轻体重,但运动量较大时,能量消耗增加,维生素和矿物质消耗也增加;膳食摄入量减少时,虽然减少了能量摄入,但同时减少了维生素和矿物质的摄入,加重维生素和矿物质的缺乏程度。儿童肥胖、抗精神病药物引起的肥胖、肥胖卧床者和肥胖2型糖尿病的治疗具有特殊性,应分别进行个体化处理。近年,对糖尿病伴严重肥胖的患者进行手术治疗获得了良好的疗效,但手术治疗的并发症较多,必须严格掌握适应证。
(二)脂质代谢病
饮食和生活习惯所致的脂质代谢性疾病相当常见,脂质代谢紊乱与高血压、肥胖、冠心病和代谢综合征的关系密切,重型肥胖与血脂谱异常已经成为许多国家的严重社会问题。由于脂肪代谢酶缺陷所致的家族性脂蛋白异常症、原发性高密度脂蛋白代谢异常、Gaucher病、脂肪酸氧化酶缺陷综合征、溶酶体脂质贮积病和过氧化物酶体病虽然少见,但其对人类健康的影响是深重的。大量的流行病学及临床实验研究表明,生活方式可通过多种环节影响血脂水平。保持健康的生活方式,无需任何经济方面的花费,而且具有肯定的降脂效果。但是,对于大多数患者来说,还需要加用降脂药物防治。临床应用较多的主要是HMG-CoA还原酶抑制剂(他汀类降脂药)和纤维酸衍生物类(苯氧芳酸类或贝特类)药物。
糖尿病血脂异常的特殊性在于出现小而密的低密度脂蛋白,胆固醇逆转运障碍,载脂蛋白糖化与脂蛋白氧化,其典型血脂谱是高甘油三酯血症伴低高密度脂蛋白胆固醇和小而密低密度脂蛋白胆固醇水平升高。其中氧化型的低密度脂蛋白更易导致动脉粥样硬化,心脑血管疾病风险远高于其他情况相似的非糖尿病患者。因此,糖尿病血脂异常的治疗目标较一般人群更严格,而不能满足于将血脂谱控制在正常范围内。
(三)蛋白质与氨基酸代谢病
此类疾病包括多种,蛋白质代谢性疾病主要有蛋白质-能量营养不良、系统性淀粉样蛋白变性和枫糖尿症;氨基酸代谢性疾病的种类很多,主要包括苯丙酮尿症、同型胱氨酸尿症、Hartnup病、酪氨酸血症、戊二酸血症和先天性高氨血症等。
1.蛋白质-能量营养不良(PEM)
是一种以机体组织不断消耗、免疫功能低下、器官萎缩和生长发育停滞为特征的多营养素缺乏综合征,而蛋白质-能量消耗综合征是PEM的一种特殊类型。PEM分为以能量供应不足为主的消瘦型(kwashiorkor),以蛋白质供应不足为主的水肿型(marasmus)和介于两者之间的混合型(mixed PEM)。营养不良(malnutrition)是一种含糊而笼统的营养概念,临床上一般根据患者的实际体重与理想体重之差进行判断。由于病程和临床类型不同,有时诊断比较困难,因而常常出现PEM诊断不足和诊断过度的两种倾向。
2.氨基酸代谢性疾病
均是先天性代谢病,多数属于常染色体隐性遗传。虽然这些疾病的诊断依据深入到了分子水平,但临床治疗仍相当困难。较有效的措施之一是避免摄入相关的氨基酸,可是在蛋白质的摄入过程中,人们无法完全避免之,治疗主要依赖于专门的特殊氨基酸制剂的供应。
【非产能物质代谢病】
(一)核酸代谢病
核酸代谢性疾病的典型例子是高尿酸血症与痛风,其与肥胖、2型糖尿病、高脂血症、高血压、动脉硬化和冠心病等密切相关,这些代谢紊乱以胰岛素抵抗为发病基础,高尿酸血症和痛风仅为其中的一种表现。
关节炎症和尿酸沉着引起急性痛风性关节炎(gouty arthritis)发作,虽然急性关节炎的症状可于数天后缓解,但由于尿酸是强烈的内源性免疫反应佐剂,可激发NOD样受体蛋白-3(NOD-like receptor protein-3,NLRP-3)活化和IL-1 介导的炎症反应,所以关节的炎症仍持续存在,而用黑皮素受体拮抗剂(melanocortin receptor agonist)阻断炎症反应可能成为新的治疗途径。慢性炎症是一组以炎症反应为特征的自身炎症性疾病(autoinflammatory disease),它与经典的自身免疫病(autoimmune disease)有本质差别,因为前者缺乏T淋巴细胞功能紊乱,而与功能异常的单核细胞半胱天冬酶-1(caspase 1)激活及IL-1β分泌有密切关系。因此,阻滞IL-1β的作用可以迅速而持久地缓解病情。表面上看来,痛风、2型糖尿病和多发性骨髓瘤并无联系,但抑制IL-1β分泌都可以收到良好的治疗效果,这一事实也再次佐证了低度炎症在一些慢性复杂病中的致病意义。高尿酸血症和痛风的治疗包括生活干预和药物两个方面。大部分高尿酸血症是可以预防的。通过节制饮食,避免大量进食高嘌呤食物,严格戒酒,防止过胖等可明显降低血尿酸水平,减少痛风发作;多饮水可以增加尿酸排出。秋水仙碱仍然是控制痛风急性发作的主要药物之一,但其胃肠道不良反应、骨髓抑制、肝功能损害、精神抑郁、神经麻痹和呼吸抑制等的严重不良反应多,老年人和敏感患者易发生秋水仙碱中毒。目前在秋水仙碱的治疗上,主张使用低剂量疗法。例如,尽早在1小时内给予1.8mg口服可以获得满意的控制效果。
新的药物制剂给急性痛风的治疗带来进步。目前的普遍做法是先用选择性环氧化酶-2抑制剂塞来昔布(celecoxib)、罗非克西(rofecoxib)、依托考昔(etoricoxib)和氯米考昔(lumiracoxib)抗炎,当常规剂量效果不佳时,可短期加用糖皮质激素;如仍无效,才考虑使用秋水仙碱。慢性高尿酸血症患者应在适当生活方式干预的基础上,使用抑制尿酸合成的药物别嘌醇(allopurinol)或非布索坦(febuxostat),或促进尿酸排泄的药物(如丙磺舒、磺吡酮、苯溴马隆和拉布立酶等)。
此外,少见的腺苷脱氨酶缺陷症、Lesch-Nyhan综合征和乳清酸尿症也属于核酸代谢性疾病的范畴。原发性核酸代谢性疾病是核酸代谢酶缺陷所致的一类疾病,高尿酸血症与痛风及Lesch-Nyhan综合征可用别嘌呤醇治疗,而腺苷脱氨酶缺陷症和乳清酸尿症尚缺乏有效的药物。
(二)代谢性骨病
临床上,代谢性骨病的诊断主要涉及三种临床表现的鉴别和病因查找,它们是高钙血症、低钙血症和骨密度减低。在绝大多数情况下,各种代谢性骨病均与上述三种临床表现有关。血钙正常的代谢性骨病主要表现为骨密度降低,极少数表现为骨密度增高。尿钙、磷、镁及其他骨生化标志物(bone biochemical marker)的异常均应与高钙血症、低钙血症或骨密度减低结合起来分析,以便进行正确而科学的诊断与鉴别。有时,代谢性骨病的诊断十分困难,而双能X线骨密度吸收法(dual X-ray absorptiometry,DXA)骨密度测定是一种巨大进步。继DXA后,近年又在定量超声(quantitative ultrasound,QUS)、定量CT(QCT)、容积定量CT(vQCT)、周围骨定量CT(pQCT)、显微CT(μCT)骨微观结构分析、有限元分析(finite element analysis,FEA)等方面有了许多进步,但这些新技术的临床应用仍存在很多疑惑,需要进行进一步的深入探讨。
和其他疾病一样,代谢性骨病的治疗应该首先去除病因,其次选用合适的有效药物控制病情。例如,二膦酸盐是一类与钙高亲和力的人工合成化合物,其骨吸收抑制活性取决于药物在骨组织的潴留量,而药物的潴留量又主要由骨转换生化标志物、肾功能和二膦酸盐的分子结构决定。因而,二膦酸盐主要用于治疗骨吸收明显增强的代谢性骨病,如变形性骨炎、多发性骨髓瘤、甲旁亢、肿瘤性高钙血症、骨纤维结构不良症、成骨不全和系统性肥大细胞增多症等;亦可用于治疗原发性和继发性骨质疏松症,主要适应于高转换型者,尤其适应于高转换型绝经后骨质疏松症又不宜用雌激素治疗者,对类固醇性骨质疏松症也有较好效果。二磷酸盐是内分泌科、骨科、肿瘤科和口腔科的常用一线药物,但各种二磷酸盐制剂的疗效和不良反应并不相同,因此,合理选择成了重要的研究课题。一般认为,阿仑膦酸钠、利塞膦酸钠、伊班膦酸钠和唑来膦酸钠的循证依据多,效果较强,副作用少。但仍偶尔发生颌骨坏死或非典型性不完全性骨折(atypical insufficiency fracture)。
以前,治疗X-性连锁显性低磷血症性佝偻病(X-linked dominant hypophosphatemic rickets)的主要方法是补充磷制剂和骨化三醇,虽然减轻症状和促进生长的效果明显,但长期治疗往往带来肾脏和其他软组织钙盐沉着、继发性甲状旁腺功能亢进症、高钙血症、高钙尿症和高血压等不良反应。如果加用西那卡塞(cinacalcet)可减少这些副作用。骨折后不愈合的预测与评估是长期困扰的临床难题,目前主要依赖于影像检查和临床检查。近来发现,Ⅰ型前胶原氨基端前肽(procollagen typeⅠ amino-terminal propeptide,PⅠNP)及其变化可以早期预测骨折后不愈合的风险,为其早期诊断与预测提供了新途径。
(三)维生素缺乏症
一般来说,维生素缺乏症是由于摄入不足、需要量增加、吸收不良或丢失过多引起。随着人们生活水平的不断提高,这些几十年前盛行的疾病已经被人们淡化,警惕性下降。但是,消化道肿瘤术后仍常常因维生素B1缺乏而出现Wernicke脑病(Wernicke encephalopathy),值得特别注意。维生素缺乏症具有以下特点:①维生素缺乏症往往属于其他原发性疾病的一种合并症或并发症,很少单独发生;②多种维生素同时缺乏的现象普遍存在;③维生素缺乏属于可预防性疾病状态,只要能维持正常饮食并在疾病状态下注意及时补充,维生素缺乏症很容易纠正。肾病时,合成1,25-(OH)2D能力减低,并进一步导致PTH高分泌、骨骼病变、异位钙化和心血管损害。因而数十年来,一直采用维生素D补充的方法来纠正代谢紊乱。近年发现,1,25-(OH)2D还具有心脏保护作用。但从现有的1653个研究报道的荟萃分析结果看,这些效果并未显现出来。当血清25-(OH)D的水平正常时,额外补充维生素D并无明确治疗效果。
叶酸和维生素B12均为DNA合成过程中的重要辅酶因子,缺乏时将造成细胞DNA合成障碍。造血细胞受累的特点是细胞核/质发育失衡,细胞核发育落后于细胞质,细胞体积大,呈现巨幼变形态。受累的红系前体细胞不能正常分化发育成熟,大部分在骨髓中原位破坏或凋亡,出现无效造血(ineffective hematopoiesis)。维生素B12缺乏所致的巨幼细胞贫血可引起神经脱髓鞘变,呈现相应的神经系统表现,但叶酸或维生素B12对人类的神经康复和认知功能没有明确影响,其原因未明,需要研究阐明。
(四)水与电解质代谢异常
由于水和电解质代谢紊乱的发生发展过程复杂,变化迅速,且相互作用,有的重叠发生,虽然水电解质代谢紊乱的诊断比较容易,但预测其变化很困难,因而,水电解质代谢紊乱与其他疾病有所不同,其诊断经常变化。同样,水电解质代谢紊乱的治疗方案亦需要根据诊断和病情进行经常调整。
1973年毕业于原湖南医学院。留校工作至今。1982年获硕士学位,1986~1988年赴德国学习,获德国医学博士学位。1993~1995年赴美国华盛顿(圣·路易斯市)从事博士后研究。1995~2001年历任湘雅二医院常务副院长、党委副书记、院长。兼任国务院学位委员会学科评议组成员,中华医学会骨质疏松与骨矿盐疾病分会副主委和后任主委,中华医学会内分泌学分会副主委,湖南医学会常务理事、内分泌学专业委员会主委,中南大学学术委员会委员,《糖尿病之友》杂志主编,《中华内分泌代谢杂志》、《中国糖尿病杂志》、《中国骨质疏松杂志》编委,1992年起享受政府特殊津贴。主持国家“九五”、“十五”、“十一五”攻关课题4项,国家自然科学基金4项,卫生部临床学科重点项目3项,教育部博士点基金2项,参与国家“973”项目2项,获湖南省科技进步奖一等奖1项,教育部科技进步奖一等奖1项,中华医学科技奖二等奖1项,国家科技进步奖二等奖1项、三等奖1项,全国优秀博士学位论文奖1项。主编《新编内科鉴别手册》、《最新临床检验手册》、《内分泌学》(上下册)、《代谢性骨病学》、《激素不敏感综合征》、《激素不敏感综合征和激素过敏感综合征》、《内分泌代谢疾病手册》和《内分泌医师手册》等专著,副主编七/八年制普通高等教育“十一五”国家规划教材《内科学》。发表研究论文285篇,其中SCI收录论文67篇,论文被引用2400余次。诊断高疑难病例287种。已培养硕士生29名,博士生36名和博士后1名。
免责声明
内容来源于人卫知识数字服务体系、人卫inside知识库,其观点不反映优医迈或默沙东观点。此服务由优医迈与胤迈医药科技(上海)有限公司授权共同提供。
如需转载,请前往用户反馈页面提交说明:https://www.uemeds.cn/personal/feedback
人卫知识数字服务体系





 Copyright © 2025 Merck & Co., Inc., Rahway, NJ, USA and its affiliates. All rights reserved.
Copyright © 2025 Merck & Co., Inc., Rahway, NJ, USA and its affiliates. All rights reserved.
