一、概述
胃癌是指发生于胃黏膜上皮的恶性肿瘤,是世界范围内最常见的恶性肿瘤之一,中国是世界上胃癌发病的大国,发病率占全球42.5%;死亡率占全球45%[1]。中国国家癌症中心公布的2015年癌症统计数据显示,胃癌位居全国癌症发病及死亡的第2位。在农村居民中胃癌发病及死亡均排名第1[2]。
胃癌的治疗进展缓慢,胃癌分型的研究从未停止,既往胃癌的临床病理分型系统主要包括Lauren分型和世界卫生组织(WHO)分型。分型依据是胃癌的形态特征、生长方式、组织结构和病理特征。但是这一类分型受到观察者个人观点与临床经验等诸多因素影响,获得的分型结果与肿瘤的实际生物学行为存在一定偏差,对临床治疗指导意义不够[3]。随着基因组学、转录组学、蛋白质组学和代谢组学等研究的开展,胃癌的分子分型逐渐成熟。
二、分子分型
肿瘤分子分型(molecular classification)的概念最早出现于20世纪90年代末,是指通过综合的分子分析技术获取更多的肿瘤信息,并在此基础上建立的新的分型[4]。自肿瘤分子分型提出以来,世界各地研究人员陆续开展了针对多种肿瘤分子分型的探讨,飞速发展的各种组学生成了海量研究数据,为分子分型提供了充足的资料。
2004年Jinawath等利用一代基因芯片技术分析胃癌基因表达谱,归纳出46个特征基因集,来区分弥漫型及肠型胃癌[5]。2011年Shah等使用基因芯片对36例局灶性胃癌样本进行差异基因表达谱分析,将胃癌分为近端非弥漫型胃癌、弥漫型胃癌和远端非弥漫型胃癌三类[6]。2011年Tan等分析了37个胃癌细胞株的基因表达谱,确定了2种内在基因亚型:基因肠型(G-INT)和基因弥漫型(G-DIF)。两种亚型与组织学Lauren分型部分一致,是独立预后因子和疗效预测因子。基因肠型预后较好,对5-FU和奥沙利铂更加敏感;基因弥漫型预后差,对顺铂较敏感[7]。
随着新一代测序技术应用到肿瘤研究中,分子分型迎来了全盛时期。2013年杜克-新加坡国立大学Lei等,对248例胃癌标本进行分析,提出了3个主要亚型(即新加坡胃癌研究组分型):增殖型(proliferative)、代谢型(metabolic)和间充质型(mesenchymal)。各亚型与Lauren分型、Tan分型有一定关系,基因特征方面不同亚型有明显特点。该研究组也对不同亚型的敏感药物进行了初探,为临床治疗用药提供了一些依据[8]。
2014年癌症基因组图谱研究协作组(The Cancer Genome Atlas Research Network,TCGA),在Nature发表了胃癌分子分型研究结果[9]。研究者对295例胃癌患者组织和血液标本进行体细胞拷贝数分析、全外显子测序分析、DNA甲基化分析、mRNA测序、microRNA测序、反相蛋白组分析(RPPA),通过对数据的整合分析,将胃癌分为四个亚型:EBV感染型、微卫星不稳定(MSI)型、基因组稳定(GS)型、染色体不稳定(CIN)型。各分型的临床特征及基因水平特征见表1。

注:PI3KCA:磷脂酰肌醇-3-激酶(PI3Ks)催化亚单位A;ARID1A:AT丰富结合域1A;BCOR:B细胞淋巴瘤因子6共抑制因子;JAK2:Janus激酶2:PDCD1LG2:细胞程序性死亡蛋白1配体2;MLH1:错配修复蛋白1;CIMP:CpG岛甲基化表型;RHOA:RAS基因家族同源物A;GTP:尿苷三磷酸;RTKs:受体酪氨酸激酶;CCNE1:细胞周期蛋白E1;CDK6:细胞周期蛋白依赖激酶6
2015年亚洲癌症研究组(Asian Cancer Research Group,ACRG)在Nature Medicine发表了一项大样本胃癌分子水平的研究数据[10]。该研究采用了新一代测序技术,累计分析了300例胃癌组织样本。通过对数据的整合分析,提出了4个胃癌分子亚型:上皮间质转化(epithelial mesenchymal transition,EMT)型、微卫星不稳定(MSI)型、微卫星稳定(microsatellite stability,MSS)/p53+型、MSS/p53-型。ACRG将该分型方法与TCGA分型、新加坡胃癌研究组分型进行比较,既有重叠又有很大不同,提示ACRG分型是一种独立的分型体系。各亚型特点见表2。
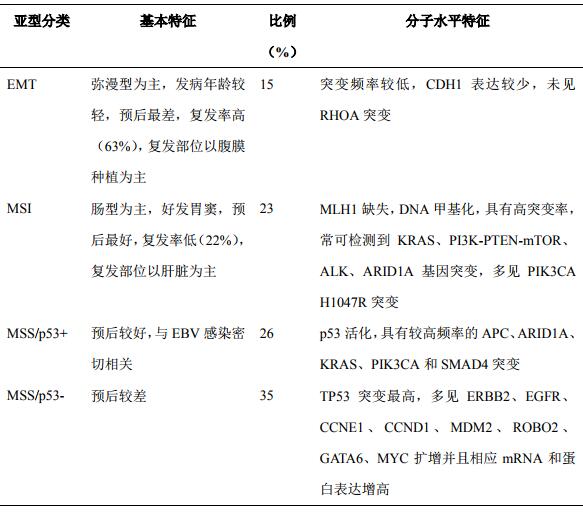
注:CDH1:钙黏蛋白1;RHOA:RAS基因家族同源物A;MLH1:错配修复蛋白1;ALK:间变性淋巴瘤激酶;ARID1A:AT丰富结合域1A
三、分子分型与临床实践
依据分子分型指导化疗药物选择的研究有许多,多属回顾性研究,存在缺乏前瞻性研究验证、结果有争议、临床应用受限等问题。Bittoni等根据Shah的分型对248例进展期胃癌进行研究,发现各类型胃癌对氟尿嘧啶为基础的两药、三药方案(铂类+氟尿嘧啶+蒽环类/紫杉醇/丝裂霉素C)的反应率不尽相同,由高到低依次是近端非弥漫型(46.1%)、远端非弥漫型(34.3%)、弥漫型(20.4%)[11]。提示根据胃癌亚型可以预测其对治疗的反应,从而更好地指导临床用药。在Tan等报道的研究中,分子亚型对不同细胞毒药物的反应也存在差异[7]。新加坡分型提示,增殖型对细胞周期抑制剂或许敏感,代谢型胃癌细胞对化疗药物5-氟尿嘧啶更加敏感[8]。
随着基因测序、生物分析技术以及大数据分析工具的出现,医学被推入精准医疗的时代。2015年1月20日美国总统奥巴马在国情咨文中宣布了精准医疗计划[12]。所谓精准医疗(precision medicine),是以基因、生物标记物、表型或心理、社会特点为基础,将相似临床表现的病人加以区分,在获得最佳疗效的同时降低不必要的不良反应[13]。既往的临床病理分型方法,不能准确反映肿瘤生物学异质性,给胃癌的治疗带来一定障碍。分子分型发展迅速,是实现胃癌精准治疗的基础。
一些早期的分子分型[6-8,14]选择的人群存在地理隔离,在代入外部数据集验证时失败,而TCGA分型、ACRG分型均经过多个群体验证,且均有不同分子分型可能的靶向治疗的提示,故而可以更大程度地指导临床实践。其中TCGA分型涉及全球患者群体,普适性良好,尽管不同亚型间的分子特征有部分重叠,但各亚型均具有相对特殊的靶向治疗通路。
1.EBV感染型:该亚型中程序性死亡配体1和2(PD-L1,PDL2)高表达、Janus激酶2(JAK2)基因扩增、磷脂酰肌醇-4,5-二磷酸3-激酶(PI3K)催化亚单位α(PIK3CA)突变,为靶向治疗提供了潜在靶点。
一项Ⅰb期研究KEYNOTE-012中,PD-1受体单抗Pembrolizumab用于治疗39例PD-L1阳性晚期胃癌患者,单药耐受良好,总有效率22.2%[15]。另一项Ⅱ期多队列研究KEYNOTE-059正在进行中,旨在评价Pembrolizumab单药与联合顺铂、5-FU治疗PD-L1阳性胃癌患者的安全性和疗效,近期报道的单个队列结果显示Pembrolizumab联合化疗耐受良好[16]。另外两项正进行的研究,试图探索同时抑制免疫检查点PD-1/PD-L1和CTLA-4/B7的治疗策略(Nivolumab+Ipilimumab,MED14734+Tremelimumab)(ClinicalTrials注册号:NCT01928394、NCT02340975)。进展期难治性胃癌患者中Nivolumab+Ipilimumab的Ⅰ/Ⅱ期研究结果显示,中位生存期6.9个月,1年生存率34%,相应的Ⅲ期研究正在筹划中[17]。
JAK通路抑制剂已进入实体瘤研究,Ruxolitinib(JAK1和JAK2抑制剂)+卡培他滨在胰腺癌研究中已显示疗效[18],Ruoxlitinib+Regorafenib在结直肠癌中的研究正在进行(ClinicalTrials注册号:NCT02119676),但目前尚未在胃癌中开展临床试验。
活化突变的PIK3CA作为一个有前景的治疗靶点,目前尚无直接靶向药物。研究发现,白人患者中该基因突变更明显[19]。PI3K通路下游mTOR和AKT是目前研究较热的靶点。口服mTOR抑制剂Everolimus,在一项未经特定分子标志物筛选的胃癌患者的Ⅲ期研究中未能达到主要终点,但是在非亚裔组中观察到了有效趋势[20]。AKT抑制剂目前有三项正在进行的研究与胃癌相关:一线GDC-0068+mFOLFOX6(亚叶酸+5-FU+奥沙利铂)的Ⅱ期研究,二线Afuresertib+紫杉醇的Ⅰb期研究,以及PIK3CA突变或扩增患者中二线AZD5363+紫杉醇的Ⅱ期研究。
2.MSI型:该亚型的基因突变率较高,表达肿瘤特异性抗原增多,加之常可见MHC-Ⅰ类基因改变,提示了免疫治疗的潜在可能。Pembrolizumab在MSI阳性结直肠癌中显示出疗效[21],关于胃癌方面的研究数据较少,前面已经做了叙述。该亚型的其他潜在靶点还包括PIK3CA、ERBB3、KRAS突变。
3.CIN亚型:该亚型是TCGA分型中所占比例最高的一型,也是涉及以往和未来靶向治疗药物最多的一型,该型多有RTK扩增基因(HER2、EGFR、MET、FGFR、VEGFA),为层出不穷的靶向药物提供了靶点。
HER2通路在胃癌中研究的非常多,自ToGA研究垫定了一线曲妥珠单抗(Trastuzumb)联合化疗治疗HER2阳性胃癌的地位[22]之后,又有一系列针对RTK的靶向药物进入研究,结果却是忧多喜少。回过头来分析失败原因,一个重要因素是没有预先对受试者进行合适的分子标志物筛选。
在HER2、HER3靶向治疗方面,一项正在进行的Ⅲ期国际多中心临床试验,旨在评价Pertuzumab(抗HER2/HER3二聚化单抗)+Trastuzumab+5-FU/卡培他滨+顺铂用于一线治疗HER2阳性晚期胃癌疗效,预计到2021年完成(ClinicalTrials注册号:NCT01774786)。另外一项Ⅱ/Ⅲ期共轭单抗-细胞毒药物TrastuzumabEmtansine(T-DM1)二线治疗HER2阳性进展期胃癌的研究,正在进行(ClinicalTrials注册号:NCT01641939)。MM-111是一种双特异抗体融合蛋白,能够结合HER2和HER3,但在一项Ⅱ期联合紫杉醇+Trastuzumab研究中因为试验组PFS劣于对照组而宣告失败。
在HER2、EGFR靶向治疗方面,Lapatinib(HER2和EGFR
双抑制剂)联合卡培他滨+奥沙利铂的一线治疗研究(TRIO013/LOGiC),以及联合紫杉醇的二线治疗研究(TyTAN)均未能达到主要终点,但是亚组分析证实试验方案对HER2基因扩增患者有一定效果[23,24]。
CIN亚型中EGFR基因扩增频率仅次于HER2,排在第2位。但在以往未行分子标志物筛选的患者中,靶向EGFR药物研究结果均未能令人满意。例如Panitumumab+表柔比星+奥沙利铂+卡培他滨一线治疗转移或局部进展食管胃结合部腺癌疗效不如单用化疗[25]。Cetuximab和Nimotuzumab与标准化疗联合均未显示获益[26-28]。EFGR酪氨酸激酶小分子靶向药Erlotinib未显示获益[29]。类似的,食管癌中EFGR酪氨酸激酶小分子靶向药Gefitinib研究[30]也未显示获益,但依据分子标志物的回顾性分析提示EGFR基因拷贝数增加的患者可能获益,这提示EGFR靶向治疗如果能进行合适的人群筛选,可能获得阳性结果[31]。
MET过表达和基因扩增均是不良预后因素,目前抗MET的单抗或其RTK抑制剂的研究均未取得预期效果,但MET信号通路仍然是值得研究药物干预的靶点。
FGFR2基因扩增也是一个可能的靶点,一些口服FGFR抑制剂尚在研究中。
AZD4547(FGFR1、2、3选择性抑制剂)的Ⅱ期研究已失败[32],一项评价Dovitinib(针对FGFR多激酶抑制剂)+多西他赛作为二线治疗的Ⅰ~Ⅱ期研究已完成,结果尚未发布(ClinicalTrials注册号:NCT01921673),另一项Dovitinib作为一、二线治疗失败后单药解救治疗的Ⅱ期研究正在进行(ClinicalTrials注册号:NCT01719549)。
CIN中存在部分或染色体的丢失[33,34],使该亚型对铂类和ADP核糖聚合酶(PARP)抑制剂敏感,在未行分子标记物筛选的胃癌二线Olaparib+紫杉醇Ⅱ期研究结果显示了总生存获益,猜想如果依据染色体不稳定检测进行患者筛选,获益可能会更大[35]。
4.GS亚型:该亚型与组织学弥漫型关系密切,具有一些独特的分子改变,包括基因突变或CLDN18-ARHGAP26融合引起RHOA信号通路异常[36,37],由于RHOA信号通路在细胞运动方面起作用,可以解释该型胃癌的弥漫浸润的特性,尽管目前尚无针对RHOA通路的靶向药物,但是这一发现为治疗弥漫型胃癌提供了启示。
综上,尽管前景非常光明,但分子分型指导药物选择仍有一段较长的路要走,需要更多的研究去发现基础研究与临床实践不匹配背后的道理。
四、讨论
胃癌分子分型,从2011年的两种,发展到2013年的三种,再到2014年、2015年的四种,取得较大的进展,有助于胃癌的分子诊断、个体化治疗、靶向药物开发,使临床胃癌患者的分组更具有指导性意义。理论上针对同一种分子变异的基因靶向治疗,比针对同一种形态类型的化学治疗更合理。故而可以预见,传统依据肿瘤表型特征决定治疗方案的做法,最终会被依据基因变异特征而进行精准治疗的模式取代[3]。
胃癌靶向治疗研究多数失败,原因值得思考。胃癌异质性强(蛋白表达、基因扩增、基因突变都可导致异质性)以及筛选患者群体是研究需关注的问题。治疗后耐药问题,分子表型如何变化,下游通路、旁路的活化和调控网络,都涉及分子水平的问题。单抗药物和小分子抑制剂的优势、劣势及如何联合应用,微环境相关治疗的发展,免疫治疗联合靶向治疗、化疗的综合治疗的发展等等,也都与分子水平的改变存在一定的关系,需要更多的研究。
一种疾病无法涵盖所有群体的特点,一种驱动基因可能揭示一群疾病的共性,分子生物学发展让我们从分子水平重新认识疾病。可以预测,胃癌乃至整个肿瘤治疗模式,将逐步转变为分子分型指导的个体化治疗,实现同病异治、异病同治以及真正意义上的精准治疗。
参考文献
1. FerlayJ, SoerjomataramI, DikshitR, et al. Cancer incidence and mortality worldwide:sourcesmethods and major patterns in GLOBOCAN 2012. Int J Cancer, 2015, 136(5):E359-E386.
2. ChenW Q, ZhengR S, ZhangS W, et al. Cancer Statistics in China2015.CA Cancer J Clin,2016.
3. 于颖彦.胃癌经典分型在分子分型时代的临床诊断价值. 中华胃肠外科杂志,2014, 17:18-20.
4. NIH. Director’s challenge:toward a molecular classification of tumors. (1999). [2016-6-23]. http://grantsnihgov/grants/guide/rfa-files/RFA-CA-98-027html.
5. JinawathN,FurukawaY,HasegawaS,et al. Comparison of gene-expression profiles between diffuse-and intestinal-type gastric cancers using a genome-wide cDNA microarray. Oncogene,2004, 23(40):6830-6844.
6. ShahMA,KhaninR,TangL, et al. Molecular classification of gastric cancer:a new paradigm.Clin Cancer Res,2011,17(9):2693-2701.
7. TanIB,IvanovaT, LimKH,et al. Intrinsic subtypes of gastric cancerbased on gene expression patternpredict survival and respond differently to chemotherapy. Gastroenterology,2011,141(2):476-485.
8. LeiZ D,TanIB,DasK, et al. Identification of molecular subtypes of gastric cancer with different responses to PI3-kinase inhibitors and 5-fluorouracil.Gastroenterology,2013,145(3):554-565.
9. Cancer Genome Atlas ResearchN. Comprehensive molecular characterization of gastric adenocarcinoma.Nature, 2014, 513(7517):202-209.
10. CristescuR,LeeJ,NebozhynM,et al. Molecular analysis of gastric cancer identifies subtypes associated with distinct clinical outcomes. Nat Med,2015, 21(5):449-456.
11. BittoniA,ScartozziM,GlampleriR,et al. Clinical evidence for three distinct gastric cancer subtypes:time for a new approach.PLoS One,2013,8(11):e78544.
12. CollinsFS, VarmusHA.A New Initiative on Precision Medicine. N Engl J Med,2015,372(9):793-795.
13. JamesonJL, LongoDL. Precision medicine--personalizedproblematicand promising. N Engl J Med,2015, 372(23):2229-2234.
14. DengN,GohLK,WangH,et al. A comprehensive survey of genomic alterations in gastric cancer reveals systematic patterns of molecular exclusivity and co-occurrence among distinct therapeutic targets. Gut,2012, 61(5):673-684.
15. BangY,ChungHC,ShangkaranV,et al. Relationship between PD-L1 expression and clinical outcomes in patients with advanced gastric cancer treated with the anti-PD-1 monoclonal antibody pembrolizumab(MK-3475) in KEYNOTE-012. J ClinOncol,2015,33:4001.
16. FuchsCS, Ohtsu,et al. Preliminary Safety Data From KEYNOTE-059:Pembrolizumab Plus 5-Fluorouracil and Cisplatin for First-Line Treatment of Advanced Gastric Cancer. J ClinOncol,2016,34:4037.
17. JanjigianYY,BendellJC,CalvoE,et al. Phase 1/2Open-Label Study of Safety and Activity of Nivolumab Alone or With Ipilimumab in Advanced and Metastatic Gastric Cancer:CheckMate 032. 2016.
18. HurwitzH,UppalN,WagnerSA,et al. A randomized double-blind phase 2 study of ruxolitinib(RUX) or placebo (PBO) with capecitabine(CAPE) as second-line therapy in patients (pts) with metastatic pancreatic cancer (mPC).J ClinOncol,2014,32:4000.
19. ChongML,ThakkarB,PangB,et al. Phosphatidylinositol-3-kinase pathway aberrations in gastric and colorectal cancer:meta-analysisco-occurrence and ethnic variation.Int J Cancer,2014, 134(5):1232-1238.
20. OhtsuA,AjaniJ A,BaiY X,et al. Everolimus for previously treated advanced gastric cancer:results of the randomizeddouble-blindphase Ⅲ GRANITE-1 study. J Clin Oncol,2013, 31(31):3935-3943.
21. LeD,UramJN, WangH,et al. PD-1 blockade in tumors with mismatch-repair deficiency. N Engl J Med,2015,372:2509-2520.
22. BangYJ,VanC E,FeyereislovaA,et al.Trastuzumab in combination with chemotherapy versus chemotherapy alone for treatment of HER2-positive advanced gastric or gastro-oesophageal junction cancer (ToGA):a phase 3open-labelrandomised controlled trial. Lancet,2010,376(9742):687-697.
23. HechtJR,BangYJ,QinSK,et al. Lapatinib in Combination With Capecitabine Plus Oxaliplatin in Human Epidermal Growth Factor Receptor 2-Positive Advanced or Metastatic GastricEsophagealor Gastroesophageal Adenocarcinoma:TRIO-013/LOGiC--A Randomized Phase Ⅲ Trial. J ClinOncol,2016,34(5):443-451.
24. SatohT,XuRH, ChungHC, et al. Lapatinib plus paclitaxel versus paclitaxel alone in the second-line treatment of HER2-amplified advanced gastric cancer in Asian populations:TyTAN--a randomizedphase Ⅲ study. J ClinOncol,2014,32(19):2039-2049.
25. WaddellT,ChauI,CunninghamD,et al. Epirubicinoxaliplatinand capecitabine with or without panitumumab for patients with previously untreated advanced oesophagogastric cancer (REAL3):a randomisedopen-label phase 3 trial. Lancet Oncol,2013,14(6):481-489.
26. LordickF,KangYK,ChungHC,et al. Capecitabine and cisplatin with or without cetuximab for patients with previously untreated advanced gastric cancer (EXPAND):a randomisedopen-label phase 3 trial. Lancet Oncol,2013,14(6):490-499.
27. SatohT,LeeKH,SunYR,et al. Randomized phase Ⅱ trial of nimotuzumab plus irinotecan versus irinotecan alone as second-line therapy for patients with advanced gastric cancer. Gastric Cancer,2015, 18(4):824-832.
28. DuF, ZhengZ, ShiS,et al. S-1 and Cisplatin With or Without Nimotuzumab for Patients With Untreated Unresectable or Metastatic Gastric Cancer:A RandomizedOpen-Label Phase 2 Trial. Medicine (Baltimore),2015, 94(23):e958.
29. DragovichT,MccoyS,Fenoglio-PreiserCM,et al. Phase Ⅱ trial of erlotinib in gastroesophageal junction and gastric adenocarcinomas:SWOG 0127. J ClinOncol, 2006, 24(30):4922-4927.
30. DuttonSJ,FerryDR,BlazebyJM,et al. Gefitinib for oesophageal cancer progressing after chemotherapy (COG):a phase 3multicentredouble-blindplacebo-controlled randomised trial. Lancet Oncol,2014,15(8):894-904.
31. PettyR,Dahle-SmithA,MiedzybrodzkaZ,et al. Epidermal growth factor receptor copy number gain (EGFR CNG) and response to gefitinib in esophageal cancer (EC):results of a biomarker analysis of a phase Ⅲ trial of gefitinib versus placebo (TRANS-COG). J ClinOncol,2017,32:4016.
32. BangY,Van CutsemE,MansoorW,et al. A randomizedopen-label phase Ⅱ study of AZD4547 (AZD) versus paclitaxel (P) in previously treated patients with advanced gastric cancer (AGC) with fibroblast Growth Factor Receptor 2 (FGFR2)polysomy or gene amplification (amp):SHINE study. J ClinOncol, 2017, 33:4014.
33. WatkinsJA,IrshadS,GrigoriadisA,et al. Genomic scars as biomarkers of homologous recombination deficiency and drug response in breast and ovarian cancers. Breast Cancer Res,2014,16(3):211.
34. MarquardAM,EklundA,JoshiT, et al. Pan-cancer analysis of genomic scar signatures associated with homologous recombination deficiency suggests novel indications for existing cancer drugs.Biomark Res,2015,3:9.
35. BangY,ImS,LeeK, et al. Randomized by ATM protein level to evaluate the efficacy and tolerability of olaparib plus paclitaxel in patients with recurrent or metastatic gastric cancer. J Clin Oncol,2015.
36. KakiuchiM,NishizawaT, UedaH,et al. Recurrent gain-of-function mutations of RHOA in diffuse-type gastric carcinoma. Nat Genet,2014,46:583-587.
37. YaoF,KausalyaJ,SiaY,et al. Recurrent fusion genes in gastric cancer:CLDN18-ARHGAP26 dinduces loss of epithelial integrity. Cell Rep,2015, 12:272-285.
主任医师、教授、博士生导师,现任北京大学肿瘤医院副院长、消化肿瘤内科主任、Ⅰ期临床病区主任、北京市肿瘤防治研究所副所长。历任中国抗癌协会胃癌专业委员会副主任委员兼秘书长,中国老年学学会老年肿瘤专业委员会执行委员会常务委员兼副秘书长,中国女医师协会临床肿瘤学专家委员会副主任委员,中国抗癌协会大肠癌专业委员会常务委员,中国抗癌协会化疗专业委员会委员, CSCO血管靶向治疗专家委员会副主任委员,CSCO胃肠间质瘤专家委员会(临床研究协作组)组长,中国胃肠道肿瘤临床试验协作组(CGOG)执行主席等。
以第一作者或通讯作者发表学术论文80余篇,其中SCI论文30余篇。作为副主编编写专著《消化道恶性肿瘤化学治疗》,作为编委参与编写专著9部。并在《中华胃肠外科杂志》《北京大学学报(医学版)》《中国肿瘤临床与康复》《中国药物警戒》、Chinese J Cancer Research、BMC Cancer、Clinical and Translational Oncology、Cancer Chemotherapy and Pharmacology、Cancer Chemotherapy and Pharmacology等学术杂志中任副主编、编委或审稿专家。
免责声明
版权所有©人民卫生出版社有限公司。 本内容由人民卫生出版社审定并提供,其观点并不反映优医迈或默沙东观点,此服务由优医迈与环球医学资讯授权共同提供。
如需转载,请前往用户反馈页面提交说明:https://www.uemeds.cn/personal/feedback
作者:沈琳教授,北京大学肿瘤医院副院长;宋刚
编辑:环球医学资讯贾朝娟





 Copyright © 2023 Merck & Co., Inc., Rahway, NJ, USA and its affiliates. All rights reserved.
Copyright © 2023 Merck & Co., Inc., Rahway, NJ, USA and its affiliates. All rights reserved.