19岁女性,无明显诱因出现发热,体温最高达39.6℃,当地医院怀疑为支气管肺炎,给予左氧氟沙星、头孢美唑抗感染治疗,患者体温未降,期间出现四肢抽搐2次,伴神志不清、双眼上翻,持续1~2分钟后自行神志转清。急查颅脑MRI平扫+增强,显示部分脑膜轻度增强,考虑为脑膜炎。骨髓涂片显示增生性贫血伴粒细胞系增多,核左移。患者遂至笔者医院住院进一步诊治。如何诊治?
一、病情摘要
1.基本情况
女性患者,19岁,以“反复发热1个月,抽搐2次”为主诉,于2015年2月入院。1个月前,患者无明显诱因出现发热,体温最高达39.6℃,无畏寒、咳痰、气促、腹痛、腹泻、头晕、头痛、尿痛。当地医院怀疑为支气管肺炎,给予左氧氟沙星、头孢美唑抗感染治疗,患者体温未降,期间出现四肢抽搐2次,伴神志不清、双眼上翻,持续1~2分钟后自行神志转清。急查颅脑MRI平扫+增强,显示部分脑膜轻度增强,考虑为脑膜炎。骨髓涂片显示增生性贫血伴粒细胞系增多,核左移。患者遂至我院住院进一步诊治。
2.既往
体质健康。
3.入院查体
体温38.9℃,脉搏116次/min,呼吸20次/min,血压135/96mmHg,体重35kg。急性面容,神志淡漠,言语稍含糊,对答尚切题,定向力、理解力尚可,计算力减退。右侧上肢肢端及左足掌面可见散在红色皮疹,直径1~4mm,压之不褪色。浅表淋巴结未触及肿大。结膜苍白,双侧瞳孔等大、同圆,直径2.5mm,对光反射灵敏。口唇苍白,颈软、无抵抗。双肺呼吸音低,可闻及少许细湿啰音。心率116次/min,律齐,各瓣膜听诊区未闻病理性杂音,无心包摩擦音。腹软,无压痛,肝、脾肋下未及。关节无肿痛,下肢无水肿,四肢肌肉无压痛,肌力、肌张力正常。病理征和脑膜刺激征阴性。
4.入院前检查
(1)实验室检查
血常规:白细胞计数(1.1~2.5)×109/L,中性粒细胞比例45.1%,血红蛋白69~75g/L,血小板计数(49~52)×109/L。血沉104mm/h。尿常规:尿蛋白阴性,尿白细胞阴性。血生化:白蛋白24~27g/L,球蛋白43g/L,ALT 82~269U/L,AST 69~332U/L,乳酸脱氢酶490~1020U/L,尿素氮7.1mmol/L,肌酐100μmol/L,钾2.6mmol/L,钠133mmol/L,钙1.77mmol/L。降钙素原0.31ng/ml。自身抗体:ANA阳性(1∶3200),抗dsDNA抗体阴性,抗SS-A阳性,抗SS-B阳性,抗Sm阴性,抗核小体阳性,抗核糖体P蛋白阳性。抗人球蛋白试验(直接法)阴性。补体C3 0.15g/L,补体C4 0.03g/L。铁蛋白618μg/L,纤维蛋白原1.92g/L,NK细胞4/μl。
(2)影像学检查
腹部B超示盆腔少量积液;心脏彩超未见异常;胸部CT示双肺弥漫性斑片状、条索状密度增高影,边缘模糊(图1)。
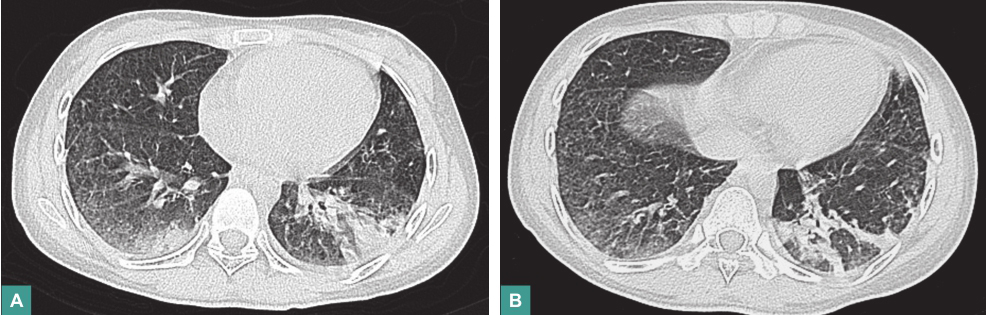
图1 胸部CT表现
(3)复查骨髓涂片
粒细胞系增多左移伴浆、组织细胞增多,有噬血现象,增生性贫血伴血小板减少(图2)。
.jpg)
图2 骨髓涂片(瑞氏染色,×1000)
5.初步诊断
①系统性红斑狼疮,神经精神性红斑狼疮可能,继发性噬血细胞综合征;②双侧肺炎。
二、诊治过程
【病例特点】
1.一般情况
患者为年轻女性,急性起病。
2.主要症状和体征
持续高热,间歇发作短暂的抽搐,神志淡漠,肢端有皮疹。
3.实验室检查
血白细胞、血红蛋白及血小板减少,肝功能损害,降钙素原轻度升高。骨髓涂片示噬血现象,抗核抗体(1∶3200)、抗SS-A、抗SS-B、抗核小体、抗核糖体P蛋白阳性,抗dsDNA抗体、抗人球蛋白试验(直接法)阴性。
4.影像学检查
胸部CT提示双肺弥漫性病变,颅脑MRI提示脑膜炎可能。
5.治疗反应
经莫西沙星、多西环素、利巴韦林、更昔洛韦多重抗感染治疗,患者症状无缓解。
【鉴别诊断思路】
根据2012年美国风湿病学会(ACR)的系统性红斑狼疮(SLE)分类标准,本例患者符合两项临床标准(白细胞减少、神经系统症状)和两项免疫学标准(抗核抗体阳性、补体下降),可诊断系统性红斑狼疮,且系统性红斑狼疮疾病活动度评分(systemic lupus erythematosus disease activity index,SLEDAI)33分,提示高度活动。患者目前主要存在神经系统、呼吸系统及血液系统(噬血现象)问题。
1.神经系统
本病例SLE诊断明确,目前的神经系统问题首先考虑神经精神性红斑狼疮(neuropsychiatric lupus erythematosus,NPSLE)可能。该病临床表现多样,包括累及中枢神经系统和外周神经系统的各种神经精神症状,癫痫样发作是其重要症状之一。由于缺少诊断金标准,确定神经精神症状为SLE所致必须严格排除其他可能的因素,可借助颅脑MRI、脑脊液检查、脑电图检查辅助诊断。SLE常合并各种感染,包括TB和真菌感染,应特别注意排查。本例患者在诊治过程中使用了喹诺酮药物(左氧氟沙星和莫西沙星),该类药物有可能加重神经精神系统的症状,应考虑调整抗感染用药方案。
2.血液系统
患者白细胞、血红蛋白、血小板进行性下降,乳酸脱氢酶明显升高,纤维蛋白原下降,高血铁蛋白,NK细胞活性下降,骨髓涂片发现噬血现象,考虑可能合并噬血细胞综合征(HPS)。自身免疫病合并噬血细胞综合征常被称为巨噬细胞活化综合征(macrophage activation syndrome,MAS),又称自身免疫病相关噬血细胞综合征(autoimmune disease associated hemophagocytic syndrome,AAHS)。它是一种特殊类型噬血细胞综合征。目前大量研究普遍认为,MAS的病理基础是多种原因引起的NK细胞活性下降或缺陷,以及细胞毒性T淋巴细胞功能缺陷,导致其不能彻底清除感染细胞,而抗原持续刺激使淋巴细胞、单核细胞和吞噬细胞过度活化,进而分泌大量炎性细胞因子,活化细胞毒性T细胞和巨噬细胞,使细胞毒性T细胞大量增殖活化,巨噬细胞吞噬功能增强,发生MAS。文献报道SLE继发MAS发生率为0.9%~5.1%。SLE合并MAS,提示病情极其危重,积极抢救或能挽回生命。
3.呼吸系统
SLE的肺部病变按发生率依次为胸膜炎/胸腔积液、间质性肺炎、肺动脉高压、小气道病变、急性狼疮肺炎、肺出血、肺挛缩综合征、肺栓塞等,常并存感染。本例患者胸部CT提示肺部弥漫性病变,暂无法鉴别其性质,可在治疗SLE的同时,积极抗感染,并密切随诊肺部情况。
【诊治措施】
1.入院后相关检查
行腰椎穿刺术,测脑脊液压力140mmH2O;脑脊液常规:脑脊液透明无色,潘迪试验阳性,白细胞计数10×106/L,淋巴细胞93%;脑脊液生化:葡萄糖4.32mmol/L,氯134mmol/L,腺苷脱氨酶7U/L,总蛋白67.0mg/dl;墨汁染色未检出隐球菌;脑脊液培养未检出细菌、真菌;脑脊液抗酸染色阴性。脑电图显示轻中度异常。
2.入院后相关治疗
予头孢哌酮/舒巴坦(3.0g,每8小时1次)抗感染,甲泼尼龙冲击(第一周500mg/d×3天,第二周1000mg/d×3天),丙种球蛋白(20g,每天1次×3天,1周后同量重复1次),续以甲泼尼龙维持量(60mg,每天1次),每周予氨甲蝶呤10mg+地塞米松10mg鞘内注射1次(共2次),环磷酰胺1000mg静脉滴注1次。经治疗,患者体温正常,皮疹消退,无抽搐、咳嗽、咳痰、胸闷,神志转清。
复查血常规变化见图3;ALT 24U/L,AST 10U/L,谷酰转肽酶119U/L,尿素氮8.2mmol/L,肌酐85μmol/L。
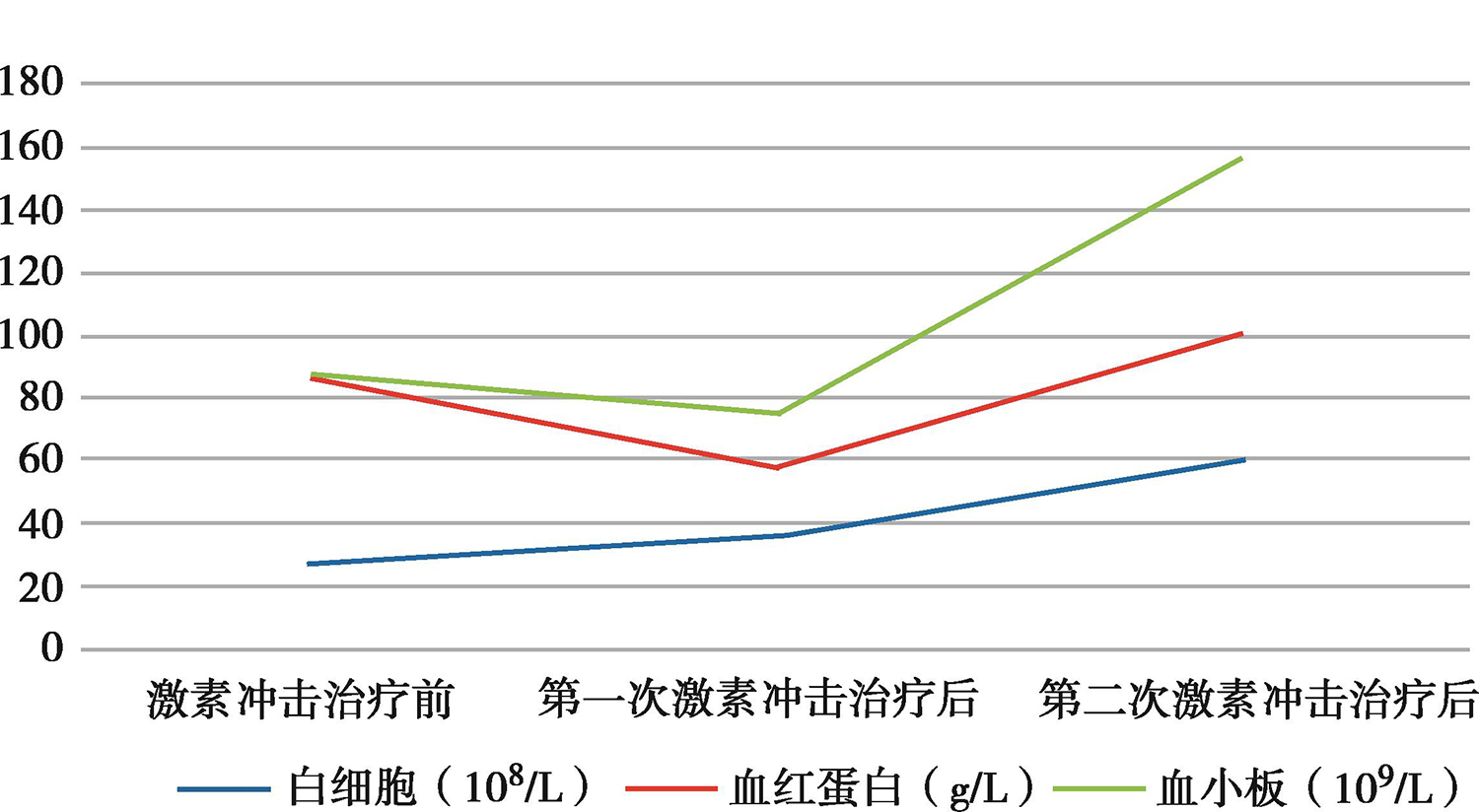
图3 血常规变化
骨髓穿刺涂片:增生性贫血伴血小板减少,未见噬血现象。
复查胸部CT:肺部病灶较前有所吸收(图4)。
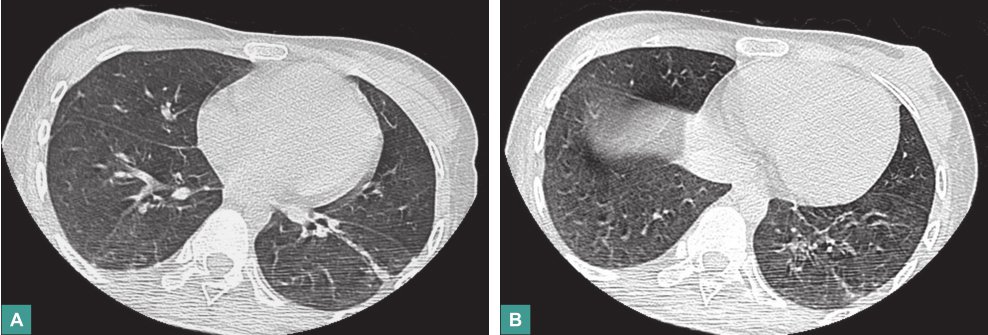
图4 胸部CT表现
环磷酰胺冲击治疗后第7天,患者再次出现发热,体温最高达39.3℃,伴恶心、呕吐、腹胀、左下腹闷痛,排黄色稀水样便3次。查体见左下腹肌紧张、压痛明显,可疑反跳痛,肠鸣音3次/min。粪便检查:黏液(+)、隐血(+),血淀粉酶266U/L,脂肪酶559.8U/L,降钙素原3.60ng/ml。
腹部立位X线平片:盆腔肠管内较多量肠内容物,未见明显气液平(图5)。腹部CT:十二指肠水平段、升段及空回肠全长管壁及相应肠系膜炎性水肿(图6)。
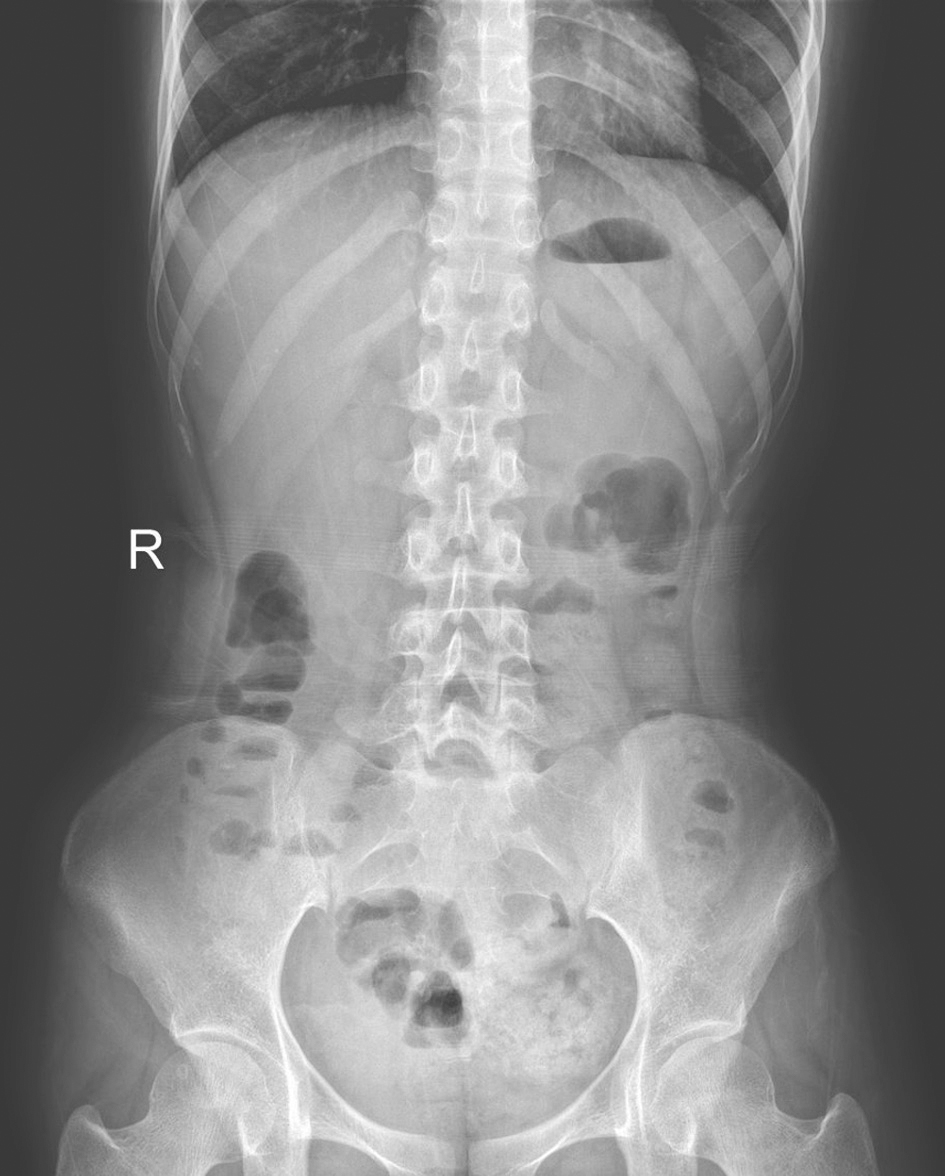
图5 腹部立位X线平片
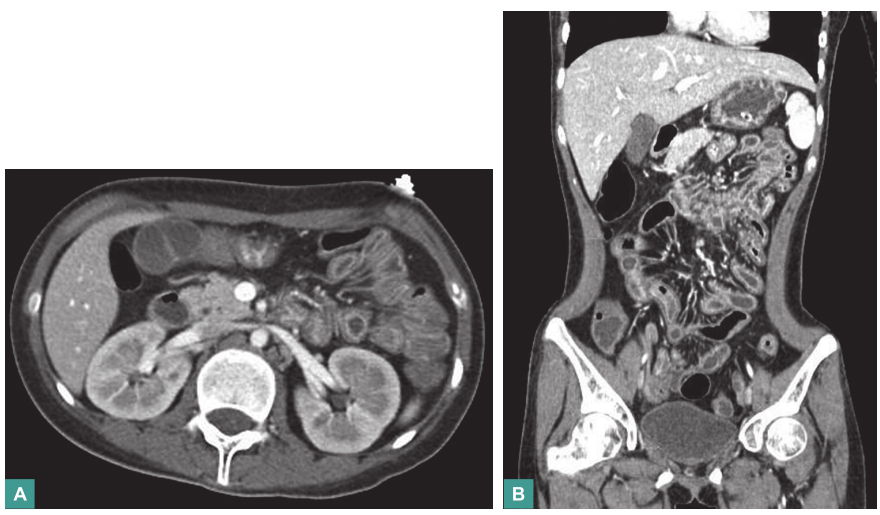
图6 腹部CT
两次大剂量激素、环磷酰胺冲击治疗后,患者出现发热、腹痛、腹泻,需要考虑SLE肠道损害及继发肠道感染两个原因。① SLE患者在疾病活动期可出现相关肠系膜血管炎引起腹痛、腹泻,甚至肠梗阻、肠坏死。腹部增强CT可见两个较为特异的征象:节段性肠管扩张,肠壁增厚水肿,肠管呈“靶形”改变;肠系膜血管充盈、增粗,呈“梳齿状”或“栅栏样”排列。本例患者腹部CT缺乏特异征象,且在大剂量激素、免疫抑制剂治疗后,出现发热、腹痛、腹泻,无法用SLE病情活动、SLE肠道表现来解释。② SLE患者本身就存在免疫紊乱,加上激素和免疫抑制剂的应用,继发感染概率高。本例患者经两次的大剂量激素冲击治疗及后续的免疫抑制剂治疗后,出现发热、腹痛、腹泻,粪便黏液(+)、隐血(+),考虑继发肠道感染可能性大。肠道感染病原体大多为革兰阴性杆菌,本病例降钙素原升高也支持革兰阴性菌感染诊断。因此,可在继续控制原发病的基础上,加用经验性抗感染治疗,同时积极寻找病原学证据。
使用头孢哌酮/舒巴坦(3g,每12小时1次)抗感染后,多次复查粪常规显示黏液(++),隐血试验(+),粪便细菌培养、大便镜检虫卵未检出病原体。治疗3天后,患者仍然持续高热(体温39℃左右),并有腹泻(排便次数8~10次/日),腹痛范围增大,累及右下腹、脐周、左上腹,粪便性状转为暗红色血便,可见黏膜状物,同时出现血压下降,最低血压60/30mmHg。经两路补液扩容、输血、用多巴胺升压[10~15μg/(kg·min)],患者血压勉强维持在90~110/60mmHg,复查降钙素原,较前明显升高(5.20ng/ml)。
抗感染治疗后,患者病情反而加重,并发生脓毒休克,提示抗菌药物未覆盖感染病原,调整用药为亚胺培南西司他丁(1g,每8小时1次)静脉滴注,病情仍未能控制。再送血培养,48小时后回报检出植生拉乌尔菌,对亚胺培南耐药。
植生拉乌尔菌属肠杆菌科拉乌尔菌属,为革兰阴性不动杆菌,可存在于动物黏膜中,致病特点与克雷伯菌相似,原发感染极少,少数病例多为免疫力严重低下者。2009年在美国发现过2株产KPC型碳青霉烯酶的植生拉乌尔菌。本病例药敏试验显示恰好为这种罕见的耐药菌。
3.最后诊断
①系统性红斑狼疮、神经精神性红斑狼疮、狼疮性血液系统损害;②继发性噬血综合征;③肠道感染;④植生拉乌尔菌败血症;⑤感染性休克。
【临床转归】
根据药敏试验结果,改用左氧氟沙星抗感染,3天后,患者体温恢复正常,腹痛、腹泻逐渐好转,升压药逐渐撤退。抗感染14天后,患者排便成形,1~2次/天,无腹痛,病情稳定出院。
患者于门诊随诊2年,一般情况好,未再发热、抽搐、腹痛、腹泻,血常规正常,血沉正常,补体正常,排便正常。
【临床难点】
本病例诊治存在以下难点:①年轻患者以高热突然发病,短时间内连续抽搐2次,血白细胞低,无SLE常见的面部蝴蝶样皮疹、口腔溃疡、关节肿痛等症状,极易被认为是颅内感染,尤其是病毒感染;②患者短时间内病情加重,全血细胞急剧减少,骨髓象出现嗜血现象,易与血液系统恶性肿瘤(如恶性组织细胞病)混淆;③NPSLE,尤其是急性发作的癫痫样症状,提示为严重的中枢神经系统病变,为SLE中的危重症,须及时做出诊断并紧急给予激素冲击治疗方能挽救生命;④HPS的发生,进一步加重了SLE的病情和不良预后,这种患者死亡率极高,治疗难度大。因此,本例患者抢救过程长,连续采取2轮超大剂量激素冲击,加上鞘内注射激素加氨甲蝶呤,同时静脉用大剂量环磷酰胺冲击,静脉应用大剂量丙种球蛋白,才使SLE病情得到控制。
在抢救过程中、病情尚未稳定时,患者发生了继发严重肠道感染,再次出现高热,并新发腹痛、腹泻,血便中见到黏膜样物质,血压下降。此种情况极易与SLE的肠系膜/肠道血管炎混淆,脓毒休克也易误诊为低血容量性休克。经密切观察、层层分析,通过多次血培养方找到极少见的条件致病菌(植生拉乌尔菌)及敏感抗感染药物,再次控制了病情。
三、点睛析评
本例患者以不典型SLE症状发病,起病急,过程凶险,属暴发型SLE,在抢救过程中继发重症肠道感染、脓毒休克,预后极差,死亡风险极高。临床医师把握关键,做出正确判断,多次送检血培养,最终找到罕见的致病菌(植生拉乌尔菌)及敏感抗感染药物,两病同治,挽救了患者的生命。
免责声明
内容来源于人卫知识数字服务体系、人卫inside知识库,其观点不反映优医迈或默沙东观点。此服务由优医迈与胤迈医药科技(上海)有限公司授权共同提供。
如需转载,请前往用户反馈页面提交说明:https://www.uemeds.cn/personal/feedback
人卫知识数字服务体系





 Copyright © 2025 Merck & Co., Inc., Rahway, NJ, USA and its affiliates. All rights reserved.
Copyright © 2025 Merck & Co., Inc., Rahway, NJ, USA and its affiliates. All rights reserved.