27岁女性,咳嗽、咳痰5个月,皮下肿块伴发热半个月。该患者多次影像学检查均提示恶性肿瘤并全身转移,而反复穿刺活检的病理结果均不支持肿瘤,所患何病?
一、病史简介
(一)一般资料
女性,27岁,2018年6月入住我院风湿免疫科。
(二)主诉
咳嗽、咳痰5个月,皮下肿块伴发热半个月。
(三)现病史
患者2018年1月受凉后出现咳嗽、咳痰,呈少量白色泡沫痰,偶有痰中带血,无发热、夜间盗汗、胸痛、呼吸困难等,抗感染治疗(具体不详)后咳嗽、咳痰症状好转。2018年3月于我院行肺部CT检查,提示“左肺占位性病变,并淋巴结、骨转移”,行支气管镜下穿刺活检,病理提示“黏膜慢性化脓性炎,肉芽组织增生;免疫组化(IgG4:2%+)”,予以多西环素0.1g,每 12h 1次,抗感染治疗1周后停药。2018年4月于我院行PET-CT检查,提示“左下肺癌并转移”,再次行CT引导下肺穿刺活检,病理提示“(左肺)慢性炎,纤维组织显著增生,伴出血”。2018年5月出现左侧眼睑皮下肿物、左侧锁骨处皮下肿物,伴午后发热、咳嗽、咳痰,最高体温40℃,其余症状同前。于当地医院就诊,考虑“成人Still病”,予以激素、沙利度胺治疗,患者仍间断低热。今为进一步诊治来我院。起病以来精神、食欲、睡眠欠佳,二便正常,体重减轻约3kg。
(四)既往史
2009年诊断“成人Still病”,曾使用泼尼松+甲氨蝶呤治疗,已停药。有“荨麻疹”病史,对“尘螨”过敏。否认肝炎、结核等传染病史,否认慢性病史,否认输血史及手术外伤史。
(五)个人史
职业是“灰指甲”治疗师,不嗜烟酒,否认疫区、疫水接触史。
二、入院检查
(一)体格检查
1.体温37.8℃,心率92次/min,呼吸20次/min,血压90/60mmHg。
2.双侧颈部及腋窝及多个淋巴结,较大者蚕豆大小,质中,无压痛。
3.左上眼睑可见一枚蚕豆大小肿物,质软,界清,无压痛。
4.左胸锁关节处可见3cm×4cm包块,边界不清,质中,有压痛。
5.双肺呼吸音清,左中肺可及少许湿啰音。
6.心脏、腹部、四肢关节均无异常。
(二)实验室检查
1.血常规 WBC 11.6×109/L,Hb 83g/L,PLT 466×109/L,中性粒细胞百分比83.1%,红细胞平均体积75.5fl,红细胞平均血红蛋白含量23.4pg,红细胞平均血红蛋白浓度309.5g/L。
2.尿、便常规均阴性。
3.肝肾功能+心肌酶学 GLO 42.5g/L,ALB 31.4g/L,ALT 133.4IU/L,余(-)。
4.PCT 示 0.24ng/ml。
5.呼吸道九联检示呼吸道合胞病毒抗体IgM(+),余(-)。
6.EBV-DNA 示11 420 IU/ml。
7.CMV-DNA、G/GM试验、输血前四项、寄生虫全套、T-SPOT、骨髓培养、痰培养均阴性。
8.新肿瘤标志物12项示 CA12-5 39.61IU/ml,余(-)。
9.免疫+风湿全套补体C4 294mg/L,补体C3 1 150mg/L,IgG 19.9g/L,IgM 3 260mg/L,CRP 99.3mg/L。
10.ESR 示113mm/h,铁蛋白 244.8ng/ml。
11.炎症因子四项 TNF-α 25.1pg/ml,余(-)。
12.狼疮全套示 ANA+S 1:80,余(-)。
13.ANA谱示抗组蛋白抗体弱阳性,余(-)。
14.骨髓穿刺、心脏彩超、腹部彩超均未见明显异常。
15.肺部CT ①左肺占位性病变,2R、4R、7组淋巴结增大,左侧第4、8前肋,右侧第4肋腋段,T10及L1椎体骨转移;②双侧腋窝下淋巴结可见,脾大,副脾(图 1)。
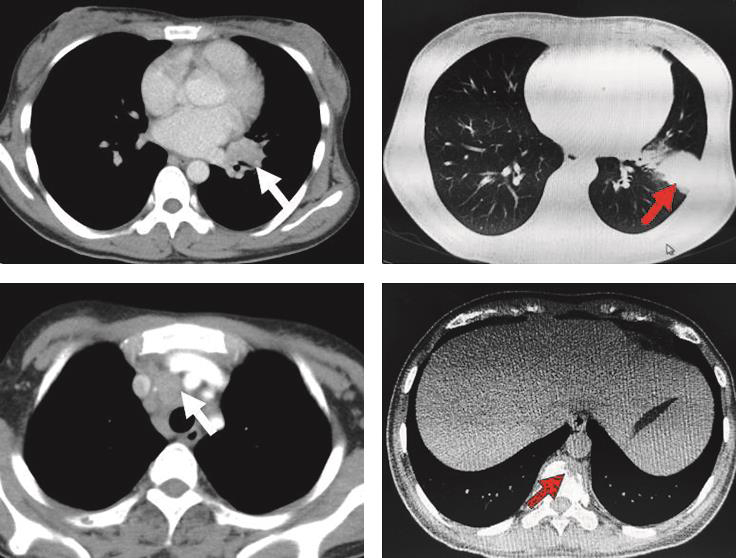
图1 肺部CT
左上:肺门肿物;右上:左肺肿物;左下:纵隔淋巴结肿大;右下:椎体破坏
16.PET-CT ①左肺下叶糖代谢异常增高肿块并周围斑片密度增高,双肺门、纵隔、双侧锁骨区、双侧腋窝、双侧颈部、肝门区及腹膜后糖代谢异常增高增大淋巴结,脾脏糖代谢异常增高结节灶,全身多发骨质密度异常伴糖代谢异常增高:考虑多为左下肺癌并阻塞性肺炎,双肺门、纵隔、双侧锁骨区、双侧腋窝、双侧颈部、肝门区及腹膜后多发淋巴结转移,脾脏多发转移,全身多发骨转移;②右侧附件区糖代谢异常增高囊实性占位:考虑为生理性卵泡摄取可能性大,必要时妇科超声检查(图2)。
17.支气管镜下穿刺活检病理 黏膜慢性化脓性炎,肉芽组织增生;免疫组化(IgG4:2%+)。
18.CT引导下肺穿刺病理结果 (左肺)慢性炎,纤维组织显著增生,伴出血。
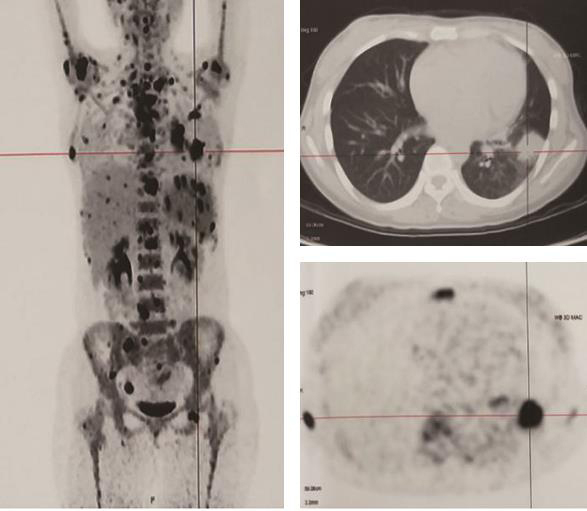
图2 全身PET-CT
三、临床分析
(一)病例特点
1.27岁,女性,病程5个月。
2.反复咳嗽、咳痰、发热。
3.肺部肿块并多发淋巴结肿大。
4.多发皮下肿块:左侧眼睑、左侧锁骨处。
5.多发骨质破坏。
6.肺部病变穿刺活检病理结果未见肿瘤依据。
7.ESR、CRP等炎症指标升高,自身抗体检查、感染病原体检查结果均无特异性。
(二)诊断分析
根据患者的临床表现及检查结果,考虑可能的诊断如下。
1.感染性疾病
(1)感染部位:
患者存在全身多处病灶,包括肺部、皮下软组织、骨骼等,考虑血行播散型感染可能性大。
(2)感染病原体
1)细菌:
患者病程慢性,一般情况较好,感染中毒症状不严重,且痰培养、骨髓培养等结果均回报阴性,考虑普通细菌感染可能性小。
2)病毒:
病毒感染多为自限性,患者病程较长,且存在多处病灶,不能以病毒感染解释,可能性小。
3)结核:
可表现为慢性病程,为低毒力感染病原体,但患者无典型的夜间盗汗、消瘦等结核消耗症状,T-SPOT检查结果阴性,痰检也是阴性,目前暂无结核证据。
4)真菌:
主要为机会致病菌,在免疫力低下的患者中,可引起深部感染、血行播散型感染,该患者曾使用过激素、免疫抑制剂治疗成人Still病,存在真菌感染的风险,完善G试验、GM试验均阴性,目前暂无真菌感染的病原学证据。
5)非典型病原体:
如非结核分枝杆菌、奴卡菌等,常见于免疫力低下患者,常为低毒力感染,表现为慢性病程,该患者临床表现及病程可以用非典型病原体解释,目前仍需要病原学证据。
2.自身免疫性疾病
IgG4相关性疾病,可以表现为炎性假瘤,血清及组织IgG4水平升高,有典型的席纹样改变、闭塞性静脉炎等病理改变,该患者表现为多处肿块,反复活检提示未见肿瘤依据,有慢性炎症的病理改变,存在IgG4相关性疾病的可能,而组织病理上IgG4比例仅占2%,不符合该病诊断;其他弥漫性结缔组织病方面,患者无典型的皮疹、关节炎、肾脏受累、血液系统受累等临床表现,无典型的自身抗体阳性,暂无依据。
3.肿瘤
该患者的多次影像学检查均提示肺部肿瘤并全身淋巴结、骨骼转移,但是反复病理活检均未发现肿瘤征相,且患者病程慢性,一般情况较好,无肿瘤的恶液质,故肿瘤可能性小。
4.其他
如结节病、卡斯尔曼病、淋巴增殖性疾病等,上述疾病均可引起全身多处肿块病灶,但需要病理证据来支持诊断。该患者反复活检,均未发现典型的病理改变,暂不支持。
四、进一步检查、诊治经过及随访
(一)病理检查
1.支气管镜下淋巴结穿刺活检
(4R、11L组淋巴结)检见大量红细胞、淋巴细胞及少量上皮样细胞,有结核可能。免疫组化CD68(+),CD56(-),LCA(+),Ki67(5%+)。抗酸染色(-)。
2.眼睑肿物病理活检
黏膜慢性化脓性炎,肉芽组织增生,纤维组织增生,伴出血。
3.锁骨处肿物病理活检
(左锁骨病灶)慢性炎,纤维组织增生,肉芽组织增生,伴充血出血,大量中性粒细胞、淋巴细胞及浆细胞浸润及少量碎骨组织,未见肿瘤;(左锁骨处软组织)慢性炎,纤维组织增生,炎细胞浸润及多核巨细胞反应,未见肿瘤。
(二)病原体检查
1.锁骨处肿物送病原体高通量检测
分枝杆菌属检出序列57个,其中石蜡分枝杆菌检出序列4个。
2.锁骨处肿物送组织培养
33天后回报“分枝杆菌属阳性”。
(三)治疗方案
利福喷汀600mg/次,每周2次;克拉霉素500mg/次,每日2次;莫西沙星400mg/次,每日1次;多西环素0.1g/次,每日1次,口服抗感染治疗。
(四)随访情况
抗感染治疗1个月后复查,患者未再发热,肺部肿块明显缩小(图3);半年后复诊,患者全身病灶均减少,无新发肿块。
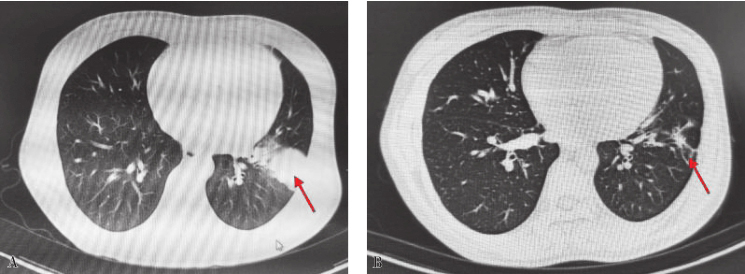
图3 肺部CT对比
(A 2018年3月治疗前肺部CT;B 2018年8月治疗后1个月复查肺部CT)
五、最后诊断及诊断依据
患者组织培养最终证实,诊断为非结核分枝杆菌感染。经过四联抗感染治疗,患者全身肿块病灶均缩小,病情好转,进一步支持该诊断。
该患者多次影像学检查均提示恶性肿瘤并全身转移,而反复穿刺活检的病理结果均不支持肿瘤,最终通过组织培养确诊为感染。于是我们产生了一个疑问——感染性疾病可以在影像学检查上(特别是PET/CT)表现为模拟恶性肿瘤的改变吗?通过文献复习,我们发现了模拟恶性肿瘤的肺部及骨髓的隐球菌感染[1]、血行播散型结核感染[2]、血行播散型奴卡菌感染[3]等多种特殊病原体感染。除了感染性疾病以外,其他非感染非肿瘤性疾病(如结节病)也可能出现类似恶性肿瘤的影像学改变[4]。
非结核分枝杆菌是一种机会致病菌,广泛分布于环境之中,发病率在(1.0~1.8)/10万[5]。根据生长速度分为快速生长型(如脓肿分枝杆菌、偶发分枝杆菌)和缓慢生长型(如胞内分枝杆菌、鸟分枝杆菌)[6]。非结核分枝杆菌感染最常见的临床表现为肺部感染,其次还可以表现为淋巴结、皮肤、软组织、骨骼及血行播散型感染[5]。
总结一下,首先感染性疾病可以在影像学上模拟恶性肿瘤;其次,结合该患者的临床表现,主要累及肺部、淋巴结、骨骼、皮肤软组织,均为非结核分枝杆菌感染常见的临床表现;最后,患者组织培养发现了该病原体,且通过积极抗感染治疗,患者临床症状改善。因此,最终诊断为非结核分枝杆菌感染。
六、经验与体会
影像学结果仅为间接证据,无论在影像学上多么支持肿瘤性疾病,最终诊断均需要得到病理证据。感染性疾病及一些少见的非感染非肿瘤性疾病可以在影像学上表现为多种多样的改变,甚至可以模拟恶性肿瘤并全身转移的征象。因此,在面对影像学支持肿瘤而病理不支持的疑难情况下,我们需要更清醒地认识到其他可能性的存在,开阔思维、寻找证据。对于可疑感染性疾病的患者,诊断需要病原学证据,若感染病灶在组织或者深部,组织培养就是必不可少的证据。在组织培养生长缓慢的情况下,借助一些快速、高通量的检测方法可以帮助我们明确诊断,并指导组织培养的方向。
免责声明
内容来源于人卫知识数字服务体系、人卫inside知识库,其观点不反映优医迈或默沙东观点。此服务由优医迈与胤迈医药科技(上海)有限公司授权共同提供。
如需转载,请前往用户反馈页面提交说明:https://www.uemeds.cn/personal/feedback
[1]WANG J,JU HZ,YANG MF. Pulmonary cryptococcosis and cryptococcal osteomyelitis mimicking primary and metastatic lung cancer in (18)F-FDG PET/CT. International journal of infectious diseases: IJID: official publication of the International Society for Infectious Diseases,2014,18:101-103.
[2]HOU S,SHEN J,TAN J. Case report: multiple systemic disseminated tuberculosis mimicking lymphoma on 18F-FDG PET/CT. Medicine,2017,96(29):e7248.
[3]ERDEMIR RU,ELRI T,SAHIN H,et al. Disseminated nocardia infection mimicking malignancy on FDG PET/CT. Revista espanola de medicina nuclear e imagen molecular,2015,34(4):268-269.
[4]ACAR T,SAVAS R,KOCACELEBI K,et al. Corticosteroid responsive sarcoidosis with multisystemic involvement years after initial diagnosis: a lymphoma mimicker on 18-FDG PET/CT. Journal of clinical imaging science,2015,5(1):40.
[5]GRIFFITH DE,AKSAMIT T,BROWN-ELLIOTT BA,et al. An official ATS/IDSA statement: diagnosis,treatment,and prevention of nontuberculous mycobacterial diseases. American journal of respiratory and critical care medicine,2007,175(4):367-416.
[6]UMRAO J,SINGH D,ZIA A,et al. Prevalence and species spectrum of both pulmonary and extrapulmonary nontuberculous mycobacteria isolates at a tertiary care center. International journal of mycobacteriology,2016,5(3):288-293.
人卫知识数字服务体系





 Copyright © 2025 Merck & Co., Inc., Rahway, NJ, USA and its affiliates. All rights reserved.
Copyright © 2025 Merck & Co., Inc., Rahway, NJ, USA and its affiliates. All rights reserved.