(一)脑膜炎
脑膜炎的诊断基于临床和实验室检查。影像学无异常发现时不能排除脑膜炎。影像学也很难作出病原学的诊断。
脑膜炎可以分为急性化脓性(细菌感染)、淋巴细胞性(病毒)和慢性(结核或肉芽肿),炎症主要累及软脑膜、蛛网膜和脑脊液。影像学主要是评估脑膜炎的继发改变:脑积水、积脓、脑炎、脓肿、继发梗死、血管狭窄和闭塞等。
CT平扫:大多表现为阴性。异常发现有脑室扩大(脑积水),脑沟脑池变浅闭塞,基底池、外侧裂、纵裂池密度增高(炎性物质积聚),儿童患者有时可见硬膜下积脓。
增强CT:显示脑沟、脑池的强化。继发的脑梗死表现低密度,CTA有时可发现血管的狭窄或闭塞。
MRI平扫:炎性渗出物集聚于脑基底池、外侧裂、纵裂池时,正常解剖结构显示不清,脑池可增宽,炎性渗出物在T1WI上为等信号,在T2WI上高信号。FLAIR上呈高信号(脑沟、脑池FLAIR高信号无特异性,还可见于蛛网膜下腔出血、伪影等)。脓肿、积脓及继发性急性梗死在DWI上呈高信号,ADC减低。
MRI增强:具有重要的价值,可见局限或弥漫的柔脑膜(软脑膜、蛛网膜)增厚强化,可伴有脑池、外侧裂内结节或环形强化灶(图1)。
伴有继发性梗死时多有大血管的受累(结核性脑膜炎常见),MRA技术能够显示血管的狭窄或闭塞。MRV技术有利于评估是否存在继发的静脉窦血栓。
脑膜炎的鉴别诊断包括:
1.癌性脑膜炎
多见于恶性肿瘤晚期。最常见原发肿瘤为乳腺癌和肺癌。少数原发性脑肿瘤也可以有脑脊液的播散,从而出现脑膜的强化,如胶质母细胞瘤、室管膜瘤、胚胎性肿瘤、生殖细胞瘤等。
2.神经结节病
多表现为“花边状”的柔脑膜强化,可伴于硬膜或脑室相连肿块。
(二)脑脓肿
脑脓肿是指脑组织的局灶性化脓性感染,是中枢神经系统最常见的感染类型。细菌、真菌、寄生虫均可引起脑脓肿。常见细菌包括链球菌、葡萄球菌、肠道细菌和厌氧菌。很多脑脓肿是混合型感染。真菌和寄生虫导致的脓肿少见,比较常见的真菌是念珠菌和曲霉菌。
脑脓肿的形成一般经历3个阶段:脑炎期、化脓期、包膜形成期。
脑炎期:早期CT平扫常表现为阴性,晚期可表现为片状低密度,边界不清。增强扫描无强化或见淡片状强化。MRI显示病灶较CT敏感,T2WI上呈稍高信号,T1WI上等或低信号。增强无或淡片状强化。DWI显示为血管源性水肿为主。病变较大时可有占位效应,表现为脑沟变浅消失和脑室受压变窄。
化脓期:病变内脑组织开始出现液化坏死,坏死灶可以一开始即较大,也可呈多发的小灶。坏死灶在CT上呈明显的低密度,在MRI上表现明显的T2高信号,信号强度高于周围炎症及水肿区。相应的坏死灶在T1WI上呈明显低信号,但信号强度高于脑脊液。此时DWI上病灶已经表现高信号。增强扫描,坏死边缘可见不完整的边缘轻度强化。多个小脓腔形成时病变可呈多房状改变。此期病变周围脑组织水肿明显,常有明显的占位效应。
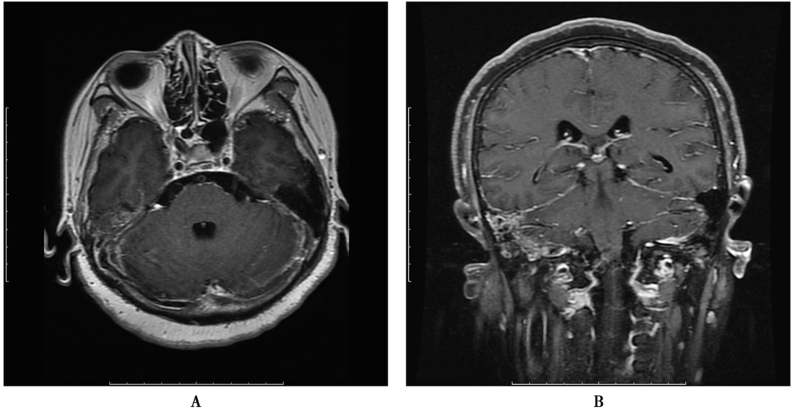
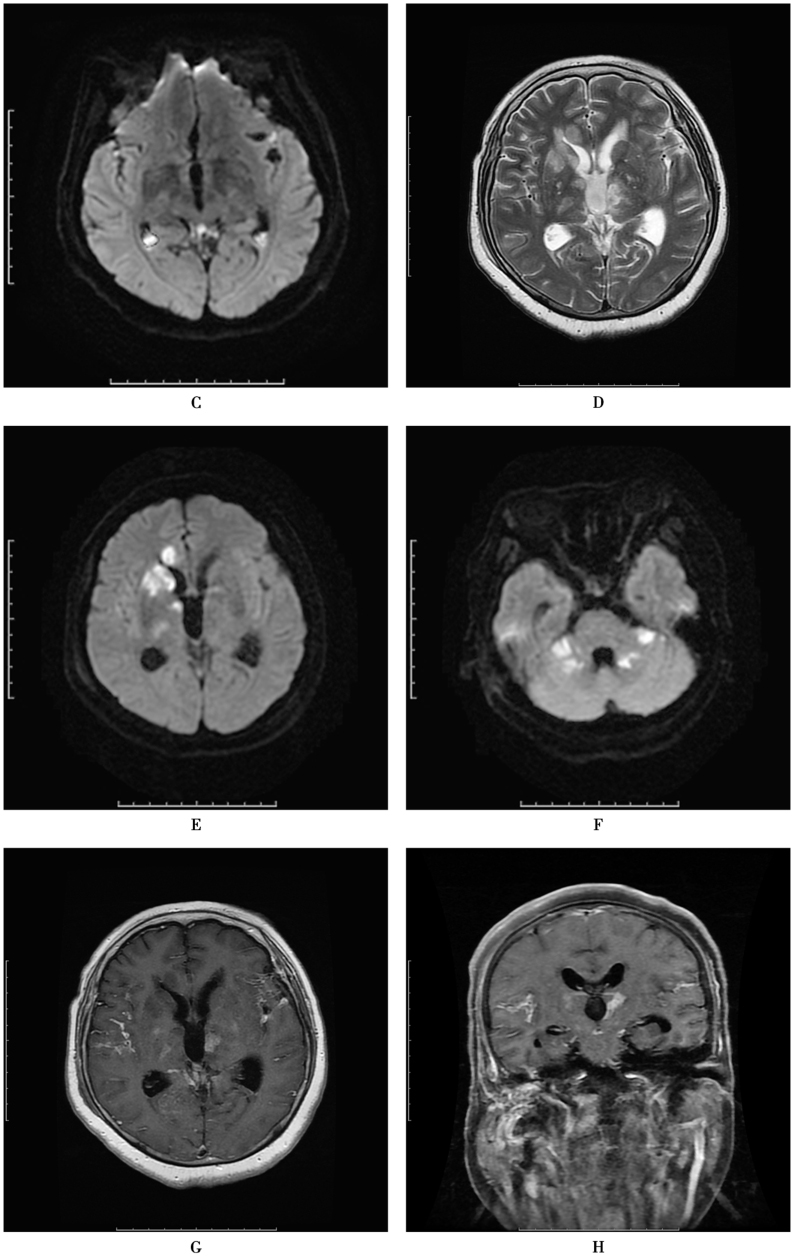
图1 化脓性脑膜炎
患者,女,62岁,发热2周,意识障碍5天。白细胞18.77×109/L,中性粒细胞百分比92.1%。血培养11小时报警:革兰氏阴性杆菌。脑脊液检查:“米汤”样,压力300mmH2O,白细胞154.61×106/L(多核86.8%),葡萄糖0.0mmol/L,氯化物108mmol/L,蛋白7.41g/L,抗酸染色(-)。随后血培养、脑脊液培养回报铜绿假单胞菌。既往史:中耳炎病史,中耳息肉切除术后。A.MRI显示右侧中耳乳突黏膜增厚,明显强化;B.脑桥周围软脑膜、小脑幕异常强化,提示炎症改变;C.幕上脑室扩张,双侧脑室后角内DWI高信号,提示积脓。D~F.1个月后复查,双侧基底节、小脑半球多发梗死灶;G、H.颅底、侧裂柔脑膜强化较前明显
包膜形成期:在坏死灶形成的同时,周围即开始有炎性细胞包绕,在此期病灶周围炎性肉芽组织开始形成包膜,称为脓肿壁,早期壁薄而不规则,后期壁厚而均匀。脓肿壁内有较多的新生血管,因此注射造影剂后可有明显的强化。脓肿的壁可以表现为外侧壁厚内侧壁略薄,这是由于脑凸面血供比深部丰富所致。脓肿周围存在子灶时,多数也是见于深部(脑室侧)。
典型脓肿壁呈3层结构:自内向外为炎性细胞反应层、胶原纤维层、胶质细胞增生层。CT上脓肿壁呈稍低密度,晚期可呈等或稍高密度。在T1WI上脓肿壁呈等或稍高信号,T2WI呈等或低信号(与壁内胶原纤维增生、出血及顺磁性自由基有关)。
脓腔在CT上呈低密度。在T2WI/FLAIR上呈高信号,T1WI上呈低信号(但高于脑脊液)。由于脓腔内有较多的细胞碎屑,水分子的弥散受限,因此DWI在脓肿的诊断中具有非常重要的价值,表现为DWI(B=1 000)上明显的高信号,ADC图上低信号。MRS可见脓腔区域醋酸盐(1.92ppm)、乳酸(1.33ppm)、丙氨酸(1.48ppm)、琥珀酸(2.4ppm)、脂峰(0.9~1.33ppm)、多种氨基酸(AA,0.9ppm)等波谱(图2)。
内科治疗有效时,脓腔缩小,脓肿壁皱缩,周围水肿减轻。但脓肿壁强化可持续数月。由于抗菌药物和激素的使用,脓肿多倾向于小环形强化灶,水肿可不明显。脓肿进展表现为脓肿扩大,水肿明显,可破入脑室形成室管膜炎,增强扫描可见脑室边缘的强化。累及脑膜形成脑膜炎。影像评价时要警惕是否伴有脑疝的形成。
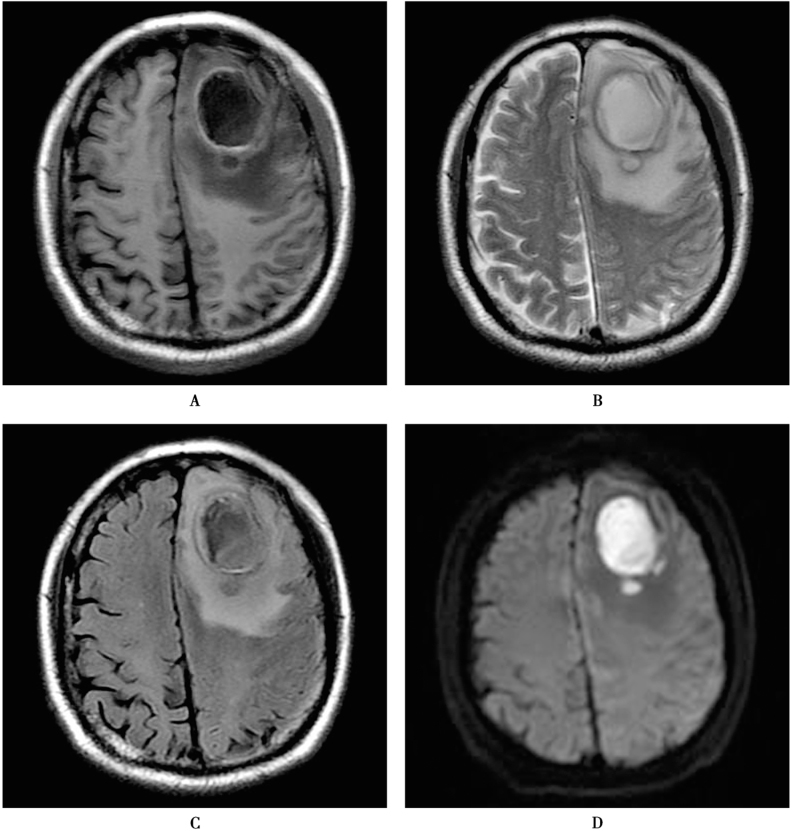
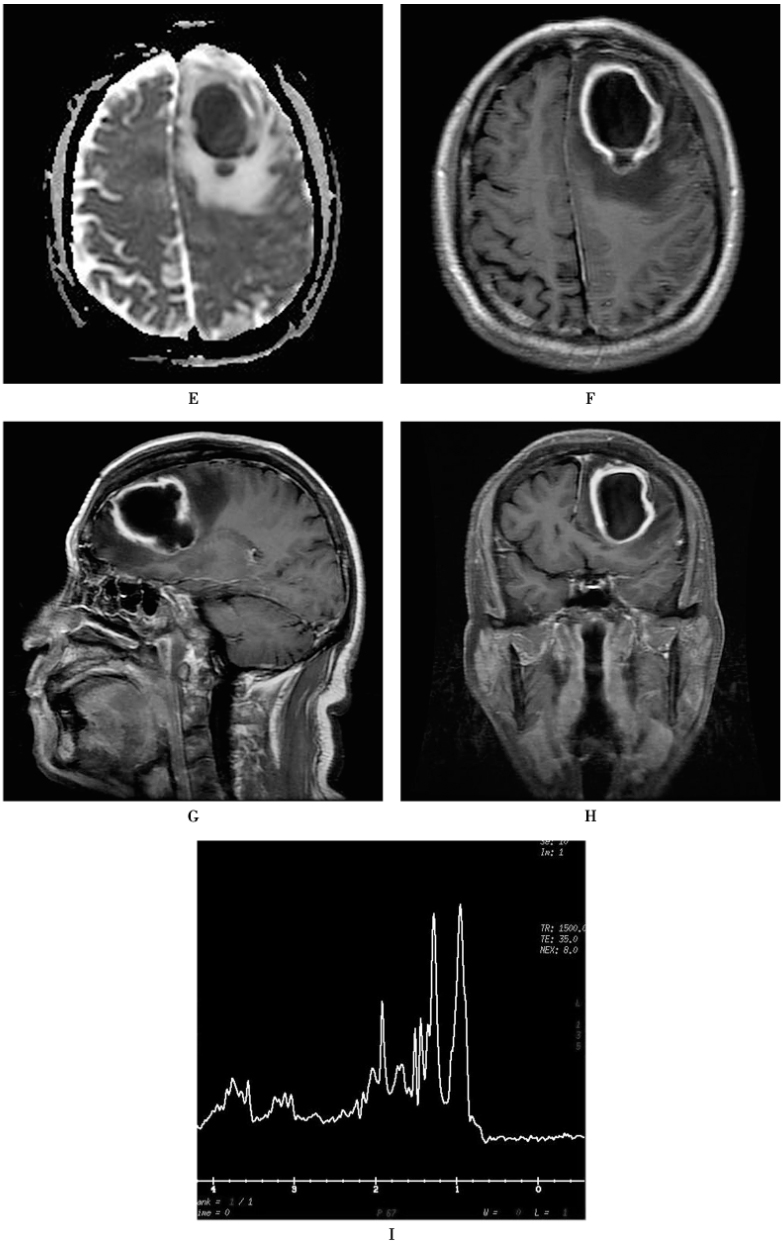
图2 脑脓肿
患者,男,67岁,突发意识障碍1天。近1周言语减少。未诉头痛、发热。外院CT发现脑内占位。白细胞:13.85×109/L。 脑脊液检查:黄色透明,细胞总数 1250×106/L,单核19×106/L,多核5×106/L,蛋白14g/L,氯化物124mmol/L,葡萄糖3.8mmol/L。手术切除病灶,术中发现腔内白色脓液,囊壁病理符合脑脓肿改变。MRI显示左侧额叶囊性占位,囊腔在T1WI(A)上呈低信号,T2WI(B)、FLAIR(C)上高信号,DWI(D)上高信号,ADC(E)减低,增强无强化(F~H)。囊壁在T1WI呈稍高信号,T2WI上等低信号,FLAIR上呈稍高信号。增强囊壁明显强化。大部分囊壁光滑,部分囊变不规则,后侧较薄,可见一卫星灶。病灶周围明显水肿,中线受压略右移。脓腔区磁共振波谱(I)可见醋酸盐(1.92ppm)、丙氨酸(1.48ppm)、脂峰(1.33ppm)、多种氨基酸(AA,0.9ppm)等波谱
影像学并不能判断脓肿的致病菌。需要密切结合临床、实验室检查,必要时需抽吸活检进行细菌培养。要积极寻找原发灶,一般脑内多发、位于皮髓交界区的脓肿提示为血行播散。感染蔓延所致脓肿多伴有脑膜炎,脓肿多数靠近感染源。注意这些征象可为临床寻找原发灶提供线索。
影像学上脑脓肿表现为环形强化灶,主要是要与肿瘤(转移瘤、胶质母细胞瘤)进行鉴别。脑脓肿的壁多数厚而均匀,内外壁光滑,病变呈类圆形有膨胀感。而肿瘤多数形态不规则,壁常厚薄不均且不光滑。DWI在脑脓肿的诊断和鉴别诊断中具有非常重要的价值。脓腔表现为DWI高信号,而肿瘤内坏死DWI上为低信号(无弥散受限)。所以怀疑脓肿时,一定要进行DWI检查。
(三)硬膜下或硬膜外积脓
脓液积聚在硬膜下或硬膜外,多为细菌性脑膜炎的并发症及鼻窦、乳突感染的直接蔓延。硬膜下积脓比硬膜外多见。脑脓肿破入脑室可见脑室内积脓。硬膜外积脓多呈梭型或凸透镜型改变,病灶多局限,CT上呈等或稍低密度。T1WI呈等信号,T2WI、FLAIR上呈高信号。增强扫描可见硬膜的强化,脓肿本身无强化。硬膜下积脓位于硬膜和蛛网膜之间的硬膜下腔隙,此间隙在大脑半球较为疏松,因此硬膜下脓肿多位于大脑半球凸面或镰旁,多呈弧形或“新月”形,范围较广。脓液CT上等或稍低密度。T1WI上等或稍低信号,T2WI、FLAIR上高信号。增强扫描可见周围边缘强化(相邻硬膜和柔脑膜)。脑室内积脓可见明显的室管膜强化。与脑脓肿相似,DWI对于积脓的诊断具有重要意义,在DWI上,脓液呈明显的高信号,ADC减低。CT积脓的诊断不如MRI敏感和特异,有时不易与慢性硬膜外/下血肿相鉴别,此时应建议MRI检查明确诊断。
亚急性或慢性硬膜下血肿、硬膜下积液:有时形态和信号特点与硬膜下积脓类似。但硬膜下积脓多有明显的临床感染症状,增强扫描可伴有柔脑膜的强化。DWI上呈高信号有利于硬膜下积脓的诊断。
(四)颅内结核
颅内结核主要由3种表现形式:结核瘤、结核性脑膜炎、结核性脑脓肿,可同时并存,单独发生时与其他感染鉴别困难。
1.结核瘤
单发或多发。CT上为等或略低密度结节。部分结节内可见周边或中心钙化是结核的特征。T1WI上结节呈等或稍低信号,部分呈高信号。T2WI上结节瘤中心干酪样坏死呈低信号,为结核肉芽肿的特征。MRI对钙化不敏感,较大钙化各序列呈低信号。增强扫描病变呈结节或环形强化。病灶周围轻度水肿,有轻度占位效应(图3)。
2.结核性脑膜炎
与其他病原体导致的脑膜炎类似。易累及脑底部(外侧裂、基底池),同时伴多发脑膜或脑实质结核结节。增强扫描脑底部脑池可见明显的强化,常伴多发结节状或环形强化(结核瘤)。并发症包括脑积水、脑水肿、梗死、血管狭窄或闭塞(图4)。
3.结核性脑脓肿
影像学表现与化脓性脑脓肿相似,影像学检查很难鉴别两者。
(五)病毒脑炎
许多病毒可感染神经系统。较常见的病毒有单纯疱疹病毒(Ⅰ型、Ⅱ型),水痘-带状疱疹病毒、巨细胞病毒、EB病毒、肠道和呼吸道病毒、HIV,以及一些虫媒性病毒如流行性乙型病毒、西尼罗河病毒等。大多数病毒感染发生于免疫缺陷的患者,影像学表现也多种多样,缺乏特异性。但部分病毒性脑炎影像学具有一定的特征。
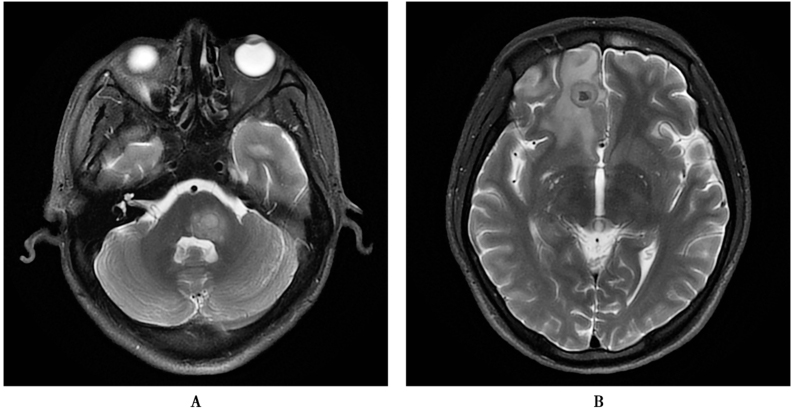
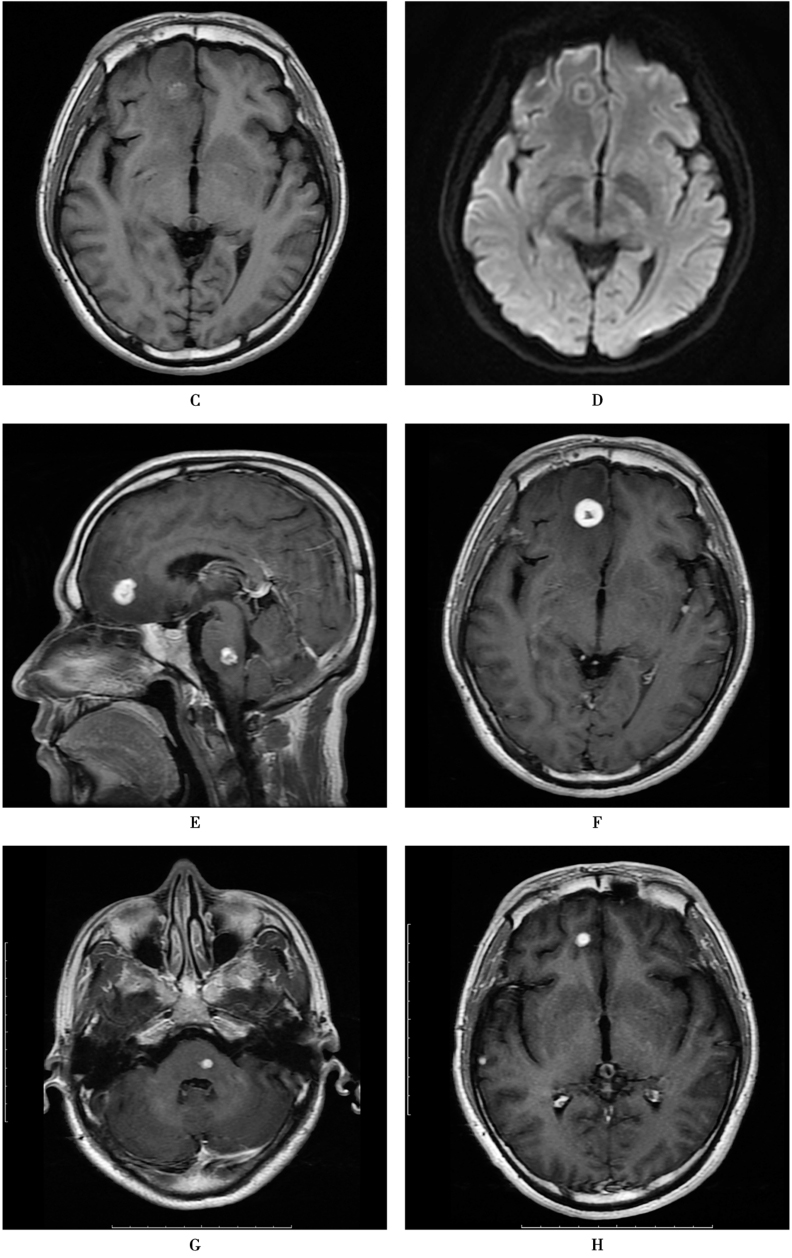
图3 结核瘤
患者,男,26岁,右手乏力7天,发热6天。胸部CT检查示“左侧大量胸腔积液”。结核/非结核分枝杆菌核酸测定:结核分枝杆菌(+),结核感染T细胞酶联免疫斑点试验(T-SPOT.TB)明显升高。脑脊液检查:细胞总数2014×106/L,白细胞总数14×106/L,单核 10×106/L,多核4×106/L,蛋白 0.64g/L,氯化物120mmol/L,葡萄糖 2.5mmol/L。 MRI显示脑干、右侧额叶各有一结节。A、B.T2WI上额叶结节中心低信号,外缘高信号,最外缘稍低信号,灶周水肿。脑干结节呈高信号;C.T1WI上右侧额叶结节稍高信号,脑干结节呈低信号;D.DWI上右额叶结节中心低信号,边缘稍高信号;E、F.增强扫描,结节呈厚壁环形强化。脑干结节边缘伴卫星灶;G、H.抗结核治疗后4个月后复查,脑干及右额叶结节均明显缩小
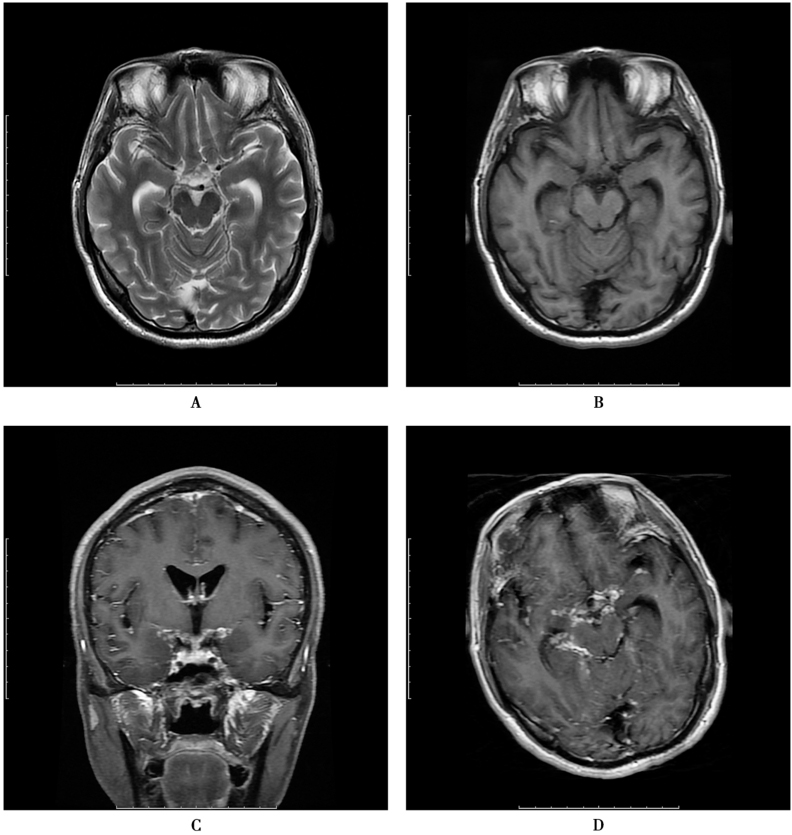
图4 结核性脑膜炎
患者,男,43岁,间断发热4个月,腹胀1个月。白细胞11.7×109/L,中性粒细胞百分比82.8%。肠镜诊断回盲部巨大溃疡。CT双肺多发粟粒结节,考虑结核。脑脊液检查:白细胞总数90×106/L,单核88×106/L,多核2×106/L,蛋白2.12g/L,氯化物109mmol/L,葡萄糖2.0mmol/L。 实验性抗结核治疗,病情好转。A、B.T2WI和T1WI显示脑室扩大,提示脑积水;C、D.增强扫描显示基底池、外侧裂柔脑膜增厚、强化,可见多发的大小不等的结节
1.单纯疱疹病毒1型脑炎
是最常见的急性重症病毒性脑炎。由1型单纯疱疹病毒感染所致,1/3为原发性感染,2/3被认为是病毒潜伏于三叉神经节或嗅神经重新激活逆行感染所致。影像学上有一定的特征性,对早期诊断具有重要价值。起病后1周内MRI的敏感性可达90%。
病变主要分布于颞叶内侧、额叶眶面,延续累及扣带回、岛叶,基底节不受累,岛叶病灶与不受累壳核分界清楚(有学者称为“刀切征”)为单纯疱疹病毒脑炎的典型特征(图5)。病变多不对称的累及双侧,但早期一般为单侧起病,随病情进展而出现对侧颞叶的受累。病变在T1WI上为低信号,在T2WI和FLAIR上呈高信号,灰白质分界不清,重者可见明显的占位效应。DWI上病变呈等或高信号,高信号代表组织的血管源性水肿,提示病变处于可恢复期。CT上早期可能不明显,其后呈现低密度改变。疾病后期或较严重时可出现点状出血,多发生于皮层,T1WI上出现脑回状的高信号。增强检查病变区可见强化,强化范围和程度随病变的时期和严重程度不同而有较大变化,轻者表现为淡片状的强化,重者出现脑回状的广泛强化,也可以出现柔脑膜强化。单纯疱疹病毒脑炎的后遗改变主要有受累脑组织的萎缩、坏死,伴信号的异常。
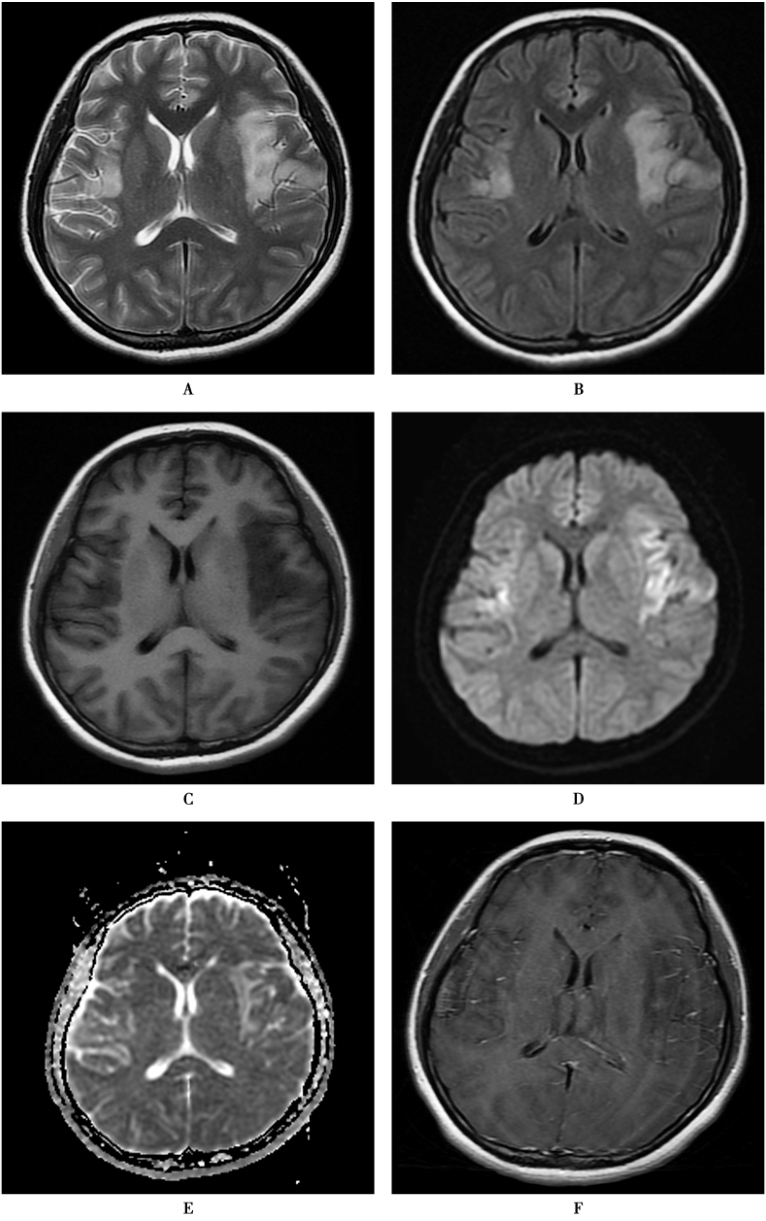
图5 单纯疱疹病毒1型脑炎
患者,女,26岁,持续性发热、恶心、呕吐伴发作性四肢抽搐意识丧失10天。最高体温40℃。白细胞13.70×109/L,淋巴细胞百分比17.1%,中性粒细胞百分比77.7%。 ESR 62mm/h。脑脊液常规检查: 细胞总数114×106/L,白细胞总数14×106/L,单核14×106/L。脑脊液生化及乳酸未见异常。细菌、真菌、墨汁、抗酸染色未见异常。脑脊液特异IgG寡克隆区带分析5项: IgG(CSF)52.90mg/L,SOB(CSF)(+),OB(CSF)(+)。 免疫组化一步法2项(AQP4.NMO)(-)。 免疫荧光病理5项 ( 脑脊液)(Hu.Yo.Ri) ( - )。EB病毒IgG/VCA(脑脊液):IgA/VCA(-),IgA/EA(-),IgG/VCA (-)IgM/VCA (-)。A、B.T2WI(A)、FLAIR(B)显示双侧颞叶、岛叶大片长T2新信号,基底节不受累,病变止于外囊呈“刀切”样改变;C.T1WI上病变呈明显的低信号;D.DWI上呈高信号;E.ADC未见减低(提示T2投射效应);F.增强扫描可见病变强化不明显,周围柔脑膜强化
病毒脑炎需要与边缘性脑炎、急性缺血梗死、低级别胶质瘤等相鉴别。边缘性脑炎多慢性发病(数周或数月),而单纯疱疹脑炎多发病急(数天),有明显的感染症状。缺血性脑梗死和低级别胶质瘤很少累及双侧。
2.日本脑炎
由流行性乙型脑炎病毒引起,最早报道于日本,因此又被称为日本脑炎。
典型的病变表现为双侧丘脑受累,CT上为低密度,T2/FLAIR上高信号。也可累及颞叶,但与单纯疱疹病毒脑炎不同,病变多分布海马的体尾部,很少累及颞叶前部和岛叶。
累及双侧丘脑的病变包括有胶质瘤、梗死、静脉窦血栓形成、中毒和代谢病,其他脑炎等,急性发病伴临床明显的感染症状如高热,要想到脑炎的可能。
(六)李斯特脑炎
单核细胞增多性李斯特菌为革兰氏阳性杆菌,兼性厌氧,无芽孢,有鞭毛及动力。能在普通冰箱冷藏室生长,是一种典型的耐冷性细菌。同时它还具有耐盐性,热耐受性较强,50℃经40分钟不能杀死,63℃加热15~20分钟死亡。易感人群食用感染的食物后,很快即可引起感染,由于李斯特菌具有嗜神经性,因此常表现为脑膜脑炎。多见于婴幼儿、老年人及免疫功能缺陷的成人患者。也可见于既往健康的青年人。
表现为脑膜脑炎时与其他病因所致脑内感染不能区分,主要靠实验室检查和临床表现。但李斯特菌易累及小脑和脑干(菱脑炎),有一定的影像特征,表现为小脑、脑干的单发或多发斑片影,边界多不清楚,T1WI上呈低信号,T2/FLAIR上呈高信号,有时表现为形态不规则的结节,周围伴有水肿。增强扫描可见多发的结节或环形强化,强化灶有时呈长条形,其内不强化部分在DWI上呈高信号(脓肿形成)(图6)。
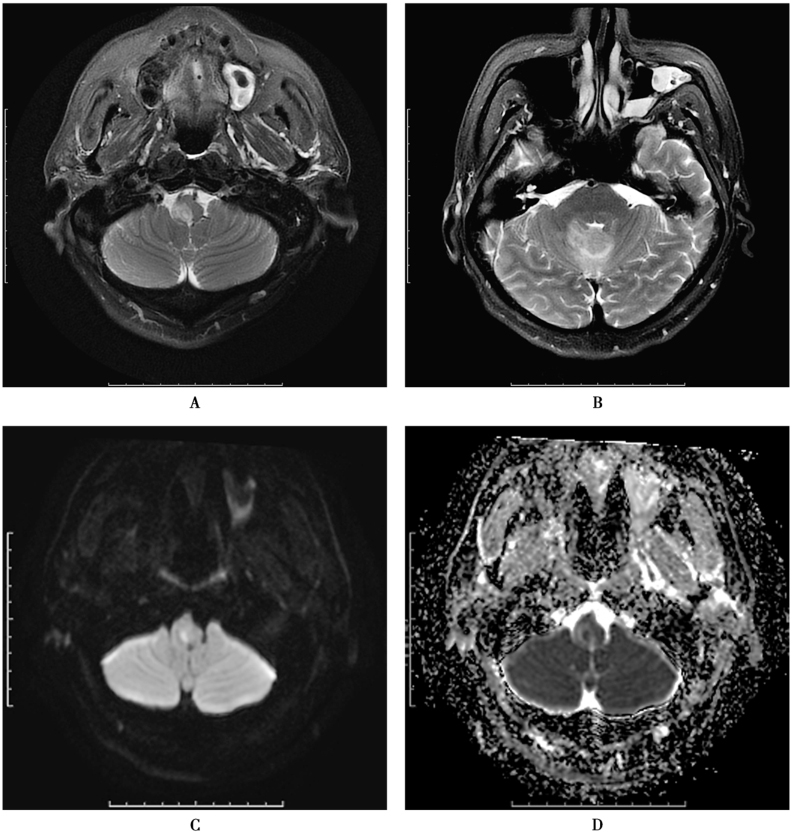
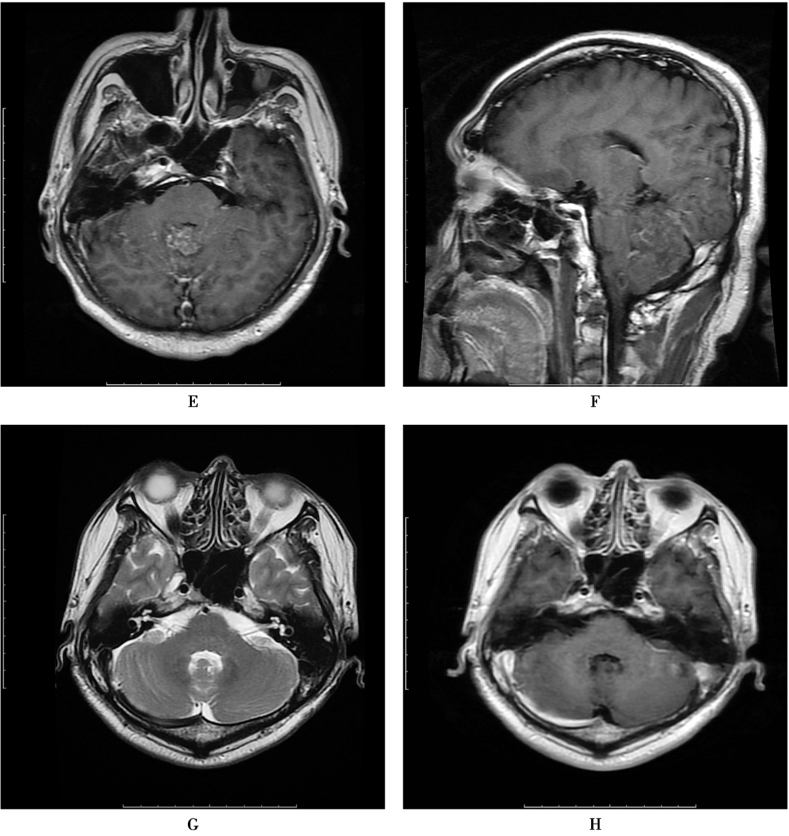
图6 李斯特脑炎
患者,男,48岁,发热10天。发病前曾食用红肠2根(冰箱冷藏)。白细胞11.4×109/L,中性粒细胞百分比75.6%↑,淋巴细胞百分比19.12%↓。脑脊液常规检查:白细胞总数84×106/L,单核75×106/L,多核9×106/L。A、B.T2WI显示右侧延髓、小脑蚓部高信号;C.DWI上右侧延髓病变内见点状高信号;D.ADC减低;E、F.增强扫描可见环形强化灶,小脑蚓部多发点状强化;G、H.治疗后复查,延髓及小脑蚓部病灶消失
李斯特菌是菱脑炎最常见的致病菌,其他感染因素包括单纯疱疹病毒、结核病、弓形虫病、隐球菌病和其他真菌感染、莱姆病、EB病毒、布鲁菌病和JC病毒等。可累及小脑和脑干的非感染性病变包括多发性硬化症、结节病、系统性风湿性疾病(Behcet综合征、系统性红斑狼疮和复发性多软骨炎)、淋巴瘤和副肿瘤综合征。要结合临床及实验室检查综合考虑。
(七)脑囊虫病
脑囊虫病是中枢神经系统最常见的寄生虫感染。囊虫(绦虫囊尾蚴)可寄居于大脑实质内、脑室内、蛛网膜下腔等部位。80%的脑囊虫寄居在脑实质内,主要位于灰白质交界处。少数位于白质深部、软脑膜、蛛网膜下腔、脑室内。
脑囊虫按演变过程可分4个时期:泡状期、胶状期、结节肉芽肿期和钙化期。
泡状期:活的囊虫,无明显脑组织炎症反应。表现为脑内多发(少部分可单发)圆形/椭圆形囊性病变,大小为5~15mm(多小于20mm),多数可见点状(1~4mm)的头节。发生于脑室内或蛛网膜下腔的囊虫可以较大,文献报道最大可达9cm。CT上头节呈等/稍高密度,囊液密度同脑脊液。边界清楚,多不伴有水肿。增强扫描无强化。MRI显示囊虫较CT更清晰,囊液信号强化与脑脊液相同,头节在T2WI/FLAIR上呈等/高信号(与脑灰质相比),T1WI上呈等/稍高信号,囊壁菲薄可不显示。
胶状期:囊虫死亡,开始退变。头节透明变性收缩,囊液变浑浊,囊壁增厚。周围脑组织炎性反应水肿明显。CT表现为厚壁囊性病变,囊内密度较高,增强扫描环形强化,头节可强化。灶周明显水肿。T1WI上囊内信号高于脑脊液,T2WI/FLAIR上呈高信号,DWI上信号同脑脊液。囊壁和头节明显强化。灶周水肿明显。部分头节退变可不显示,仅显示厚壁环形强化。
肉芽肿期:囊液吸收,囊肿缩小直至形成纤维结节,周围组织水肿仍然存在但开始减轻。增强扫描囊灶缩小,呈环形或结节状强化。灶周水肿减轻。
钙化期:囊虫死亡,钙盐沉积。CT上表现为小钙化灶。MRI显示钙化不如CT敏感(图7)。
脑室内囊虫多见于第四脑室,可以导致室管膜炎和脑积水。脑池内囊虫可以表现为葡萄状改变,通常不显示头节。在儿童,脑囊虫病有时呈“脑炎”样改变(多发小强化病灶伴大面积水肿)。
Del Brutto等2017年更新了神经囊虫病的诊断标准。在这个新的标准中,神经影像学有绝对标准:典型的囊+头节,有此征象可确诊脑囊虫病。主要标准:没有头节的囊;单个或多发的环形/结节状强化灶;蛛网膜下腔多发囊泡;典型脑内多发钙化灶。确认标准:抗囊肿药物囊性病灶缩小;单个增强灶的自发吸收;囊性病灶在脑室内移位。次要标准:梗阻性脑积水或颅内软脑膜异常强化。主要标准、确认标准和次要标准要结合临床及实验室检查才能诊断囊虫病。
胶状期囊虫需要与肿瘤、脑脓肿、结核等相鉴别。脓肿DWI上囊内为高信号。肿瘤囊壁多不规则。结核瘤多同时伴有脑膜炎。
(八)其他寄生虫
1.裂球蚴
裂球蚴虫体在脑组织内形成移动造成不规则的坏死隧道、周围炎症反应。典型影像学表现为隧道样强化。随访部分病灶可见强化灶的形态和位置发生变化(虫体移动)。
2.包虫病
细粒棘球蚴导致囊性包虫病,包囊边界清晰,囊液同脑脊液信号/密度,母囊内可见多个子囊,周围无明显水肿带,可单发或多发;包囊破裂可见强化,周围出现水肿带。泡状棘球蚴感染又称脑泡性包虫病,浸润性生长,T2WI上病灶呈低信号,内有多个稍高信号小囊泡影,有不规则强化,周围水肿明显。
3.其他
其他多种寄生虫均可导致神经系统感染,多数有斑片或环形、结节样强化,伴周围水肿。影像学表现缺乏特异性。
(九)真菌感染
神经系统的真菌感染比较少见,主要见于免疫功能低下的患者。部分类型的真菌也可感染免疫功能强的患者,如隐球菌、组织胞浆菌等。感染形式主要是血型播散或直接蔓延。也可见外伤、手术后等。真菌感染可形成脑膜炎、脑脓肿,肉芽肿,易侵犯脑动脉继发梗死、脑炎、真菌性动脉瘤、甚至脑出血等。侵犯静脉系统可形成静脉窦血栓。在免疫功能低下的患者,真菌可能不导致机体的免疫反应,临床和影像学表现均可无明显异常。
1.隐球菌感染
是AIDS患者比较常见的真菌感染。多由呼吸道感染血行播散所致,播散到脑膜导致隐球菌脑膜炎。进一步向皮层侵犯可形成脑实质感染。隐球菌性脑膜炎的影像学表现不明显。CT通常无阳性发现,偶见萎缩和脑积水。MRI也可见阴性表现,但较CT敏感,增强扫描可见脑膜的明显强化。脑实质感染表现多样,有几种形式:血管周围间隙增宽、凝胶样囊肿、脑实质/柔脑膜肉芽肿及混合形式。脑血管周围间隙扩大是隐球菌及其分泌的黏液样物质积聚导致的。多位于基底节、中脑,也可见于整个脑组织。增强后无明显强化。病变进一步发展,脑血管周围间隙扩大可聚集较大的囊肿,其内可见分隔。囊内为黏液、胶状物质充填,内含大量隐球菌,多发的囊肿呈肥皂泡状(soap bubble appearance)改变,具有一定的特征性,囊肿周围可有或无水肿,一般无强化(图8)。肉芽肿形成时可表现脑实质/脑膜的结节,主要分布于双侧基底节区及侧脑室旁。病理上为慢性肉芽肿反应,包含巨噬细胞、淋巴细胞和异物巨细胞浸润,伴血脑屏障破坏。CT上结节密度可较高。T1WI上呈等、低信号。T2WI呈高信号。增强后呈明显的结节状、环形强化,多发病变可呈串珠样改变。病灶周围可见水肿。其他继发改变包括脑积水、继发性梗死(隐球菌血管炎)、脑萎缩等。
2.毛霉菌感染
脑毛霉菌感染是最为凶险的中枢神经系统真菌感染,可致命。糖尿病和铁超载是毛霉菌感染的高危因素。糖尿病患者常伴鼻窦、眼眶感染,罕见肺部或播散型感染。使用激素或中性粒细胞减少的患者毛霉菌感染常由肺部毛霉菌感染血型播散或鼻窦眼眶感染直接侵犯。

图7 脑囊虫病
患者,男,36岁,间断头痛3个月余。腰椎穿刺提示脑脊液压力200mmH2O,白细胞总数34×106/L,单核32×106/L,蛋白0.86g/L↑,囊虫IgG(+)。A.T2WI显示右侧基底节区囊性高信号,囊壁低信号,周围水肿;B.T1WI上囊腔低信号,囊壁稍高信号;C.DWI上囊腔低信号;D.增强扫描囊壁环形强化,另可见左侧基底节、右侧岛叶小结节,轻度环形强化;E、F.CT见右侧基底节区病变显示不明显,其他小结节钙化,右侧额叶皮层下见点状钙化
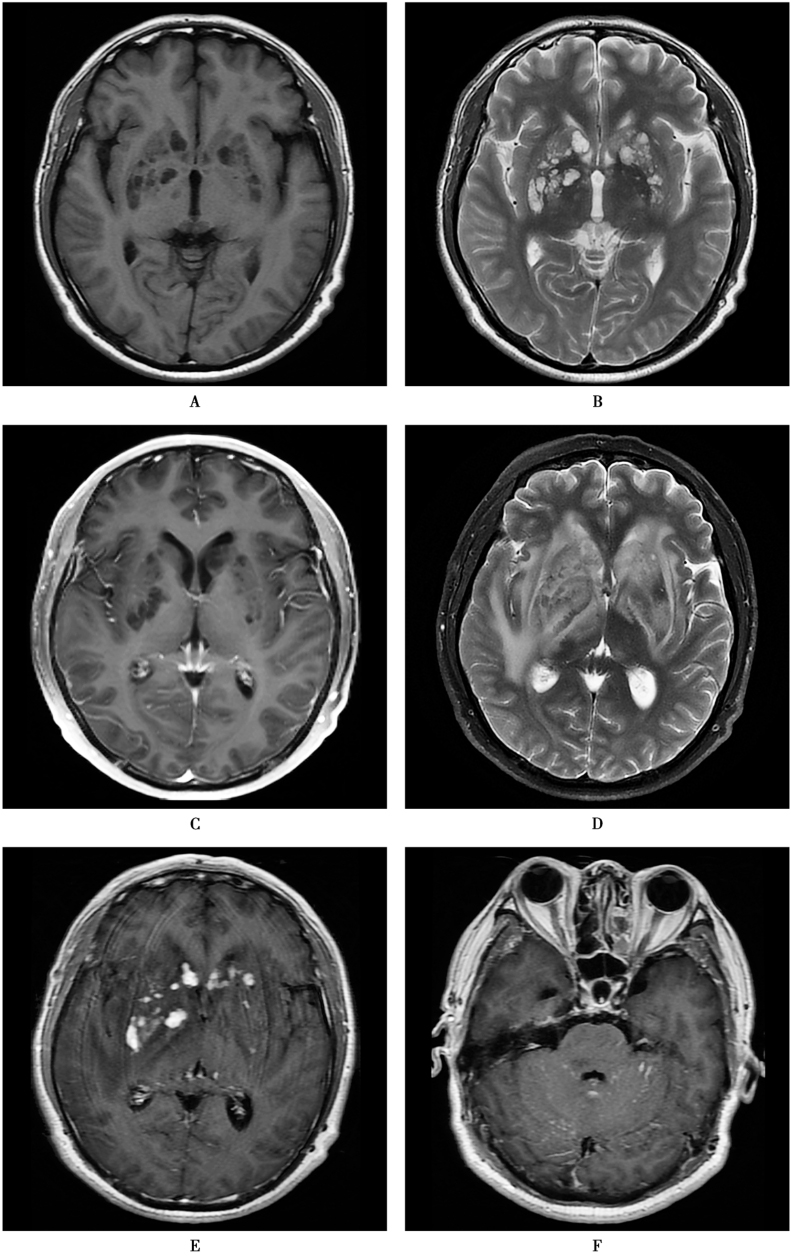
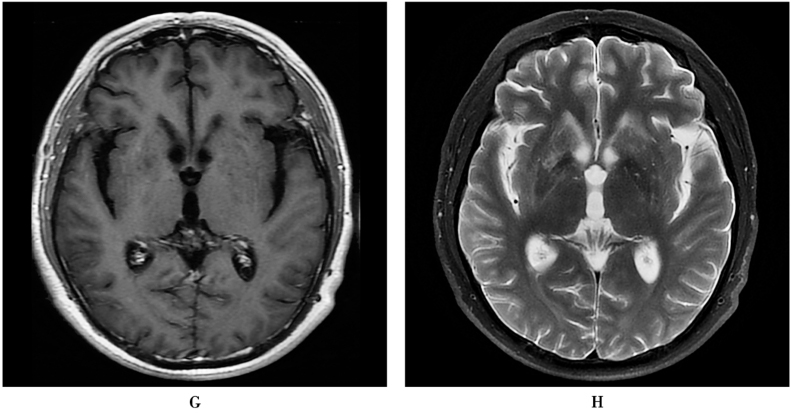
图8 隐球菌感染
患者,男,31岁,头痛21天。无明显诱因出现持续性全头痛,剧烈疼痛,呈爆炸感,伴有恶心、呕吐,呕吐呈喷射状,呕吐物为胃内容物,无发热、抽搐、意识障碍等。腰椎穿刺测压力>330mmH2O。脑脊液检查:外观透明,细胞总数 283×106/L,白细胞总数 176×106/L,单核 95×106/L,葡萄糖 2.2mmol/L,氯化物114mmol/L,蛋白0.84g/L。脑脊液隐球菌抗原≥1∶1024。脑脊液IgG寡克隆区带(+),特异IgG寡克隆区带(+),IgG 159.0mg/L(参考值10.0~40.0mg/L)。2015年11月MRI显示双侧基底节区多发囊性病变,大小不一,较大病灶内见分隔;A.T1WI上低信号;B.T2WI上高信号;C.增强无强化。D~F.2016年10月治疗后复查,显示囊性灶演变为强化结节,周围水肿明显,同时小脑半球柔脑膜多发微小结节状强化。G、H.2017年6月再次复查,显示病灶明显吸收,大部分消失
鼻-脑型毛霉菌病多由鼻窦霉菌经筛板沿血管和神经周围通道进入额叶,或经眶尖进入海绵窦。与其他感染相比,筛窦的毛霉菌感染可影响侵袭途径中的全部结构,包括眼眶、眼球、骨和脑组织。由于筛窦的静脉与海绵窦相通,因此筛窦毛霉菌感染诱发海绵窦血栓形成的风险较高。无论直接蔓延还是血型播散,霉菌进入脑内多累及大脑或小脑基底部导致颅底脑膜炎和真菌性脑脓肿。可侵犯血管导致血管狭窄闭塞,继发出血或缺血性梗死。MRI评价颅底病变较CT敏感。鼻窦炎可仅表现为黏膜增厚,晚期可见液平面和骨质破坏。增强扫描颅底可见脑膜增厚强化及结节或边缘强化灶(脓肿)。
3.其他真菌
真菌感染多导致脑膜炎(多见于颅底)、肉芽肿、脑脓肿、脑积水,常累及动脉,继发缺血性梗死或出血。影像学表现多无特异性。
神经系统的真菌感染多无特异性,诊断困难。免疫功能低下的患者脑内出现不典型的脓肿、脑膜炎、出血性梗死等要考虑到真菌的可能。诊断要结合临床和实验室检查。
(十)神经梅毒
神经梅毒可发生于梅毒感染的各个阶段,但多为晚期梅毒全身损害的重要临床表现,可以分为无症状梅毒、脑膜血管型梅毒、脑实质型梅毒(麻痹性痴呆、脊髓痨)、树胶肿型梅毒及多发性神经根神经炎等。
影像学:无症状梅毒和多发性神经根神经炎常规神经影像学多无异常表现。
急性梅毒脑炎:早期神经梅毒常表现为脑膜炎,CT和MRI平扫可能无异常发现,增强扫描可以显示局灶性或弥漫性的柔脑膜强化,累及颅内神经时可见强化,常见于面听神经(第Ⅶ和Ⅷ脑神经)。影像学并不能区分梅毒和其他感染(如结核、结节病等)导致的脑膜炎。
少数病例表现为大面积的长T1长T2信号,类似于单纯疱疹病毒脑炎改变(图9),可能代表了脑组织的炎症和水肿,与脑膜受累有关,增强扫描柔脑膜强化,对提示诊断有重要帮助。
如果存在树胶肿(是梅毒螺旋体侵入中枢神经系统后于硬脑膜或软脑膜处出现强烈的局限性炎症反应而形成的肿块样病变,多见于Ⅲ期梅毒患者)则表现为邻近脑膜的小结节(单发或多发),CT上等密度。T1WI低或等信号。T2WI、FLAIR上呈高信号,或高、等、低混杂信号,DWI上常表现为高信号,ADC也呈高信号。增强扫描表现为均匀的结节状强化或环形强化,偶尔伴有脑膜尾征。多伴有斑片状的脑膜炎和明显的水肿。结节较大,伴有中心坏死时,影像学表现可以与肿瘤或脓肿相似。

图9 神经梅毒
患者,男,48岁,性格改变1年余,言语不清,抽搐15天,意识障碍3天。快速梅毒血浆反应素试验(RPR)(脑脊液):RPR(+),TPPA(+)。 快速梅毒反应素(RPR)滴度(脑脊液):RPR 1∶16 (+)。快速梅毒反应素(RPR)滴度(血):RPR 1∶32(+)。A、B.T2WI和FLAIR显示左侧颞叶、岛叶、双侧海马大片高信号;C.T1WI上呈明显的低信号;D.DWI上病变呈稍高信号,ADC稍高;E.T2WI病变呈高信号,未见出血低信号;F.CT显示左侧颞岛叶大片低密度
累及脊髓时,则表现为脊髓内长阶段的异常信号(T2WI上高信号),脊髓肿胀,病灶多位于脊髓中央(横断面),但可以累及后部。多见于胸段脊髓。增强可见结节状或斑片状强化。
脑膜血管型神经梅毒:梅毒累及脑内大血管,形成血管内膜增生,导致管腔狭窄和继发扩张。累及小血管,导致血管闭塞及继发性缺血性梗死。DSA、CTA、MRA可以发现大中动脉的狭窄和狭窄后扩张及闭塞,可见远端分支减少。DWI可以发现急性和亚急性期梗死灶。脑实质型梅毒:又称麻痹性痴呆。影像学表现可以正常。但多有不同程度的弥漫脑萎缩。可伴有皮层和基底节多发的小斑片影,T1WI上等或稍低信号,T2WI、FLAIR上高信号。部分患者可出现脑室旁的白质弥漫性病变,表现为T2WI、FLAIR上高信号,多位于侧脑室旁。但这些表现缺乏特异性(图10)。
神经梅毒的诊断主要是依靠临床和实验室检查。影像学主要是作符合性诊断。影像学表现正常不能排除神经梅毒。有异常时要与其他相似表现的疾病进行鉴别。如树胶肿要与肿瘤、肉芽肿、脑脓肿等相鉴别。脑膜血管性梅毒则要与脑炎、脑梗死等相鉴别。
(十一)艾滋病患者脑部感染
艾滋病患者免疫功能低下,可疑合并多种机会性感染,包括病毒、真菌、弓形体,还可以合并淋巴瘤。
1.HIV脑炎
HIV对神经组织有亲和性,可直接侵犯脑实质和脑膜,引起非化脓性脑炎和/或脑膜炎。影像学表现主要是双侧大脑半球白质对称性病变,主要分布于侧脑室旁和额顶叶深部白质,多融合呈大片状,无占位效应。CT上呈低密度,T1WI上呈低信号,T2WI/FLAIR上高信号。可见不同程度的脑萎缩改变,表现为脑沟增宽,脑回变薄。
2.弓形体脑炎
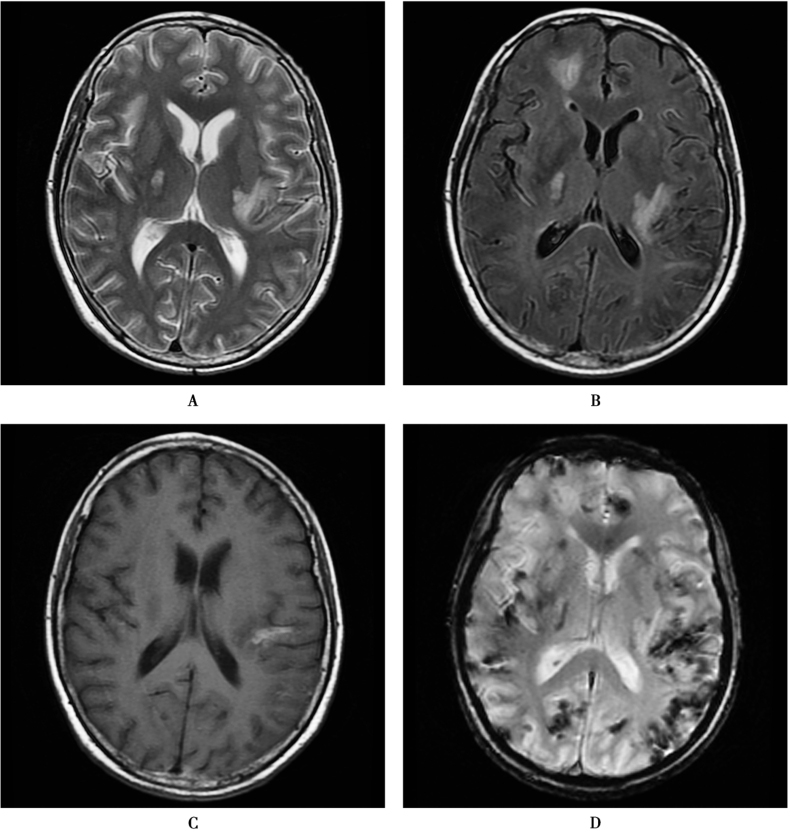
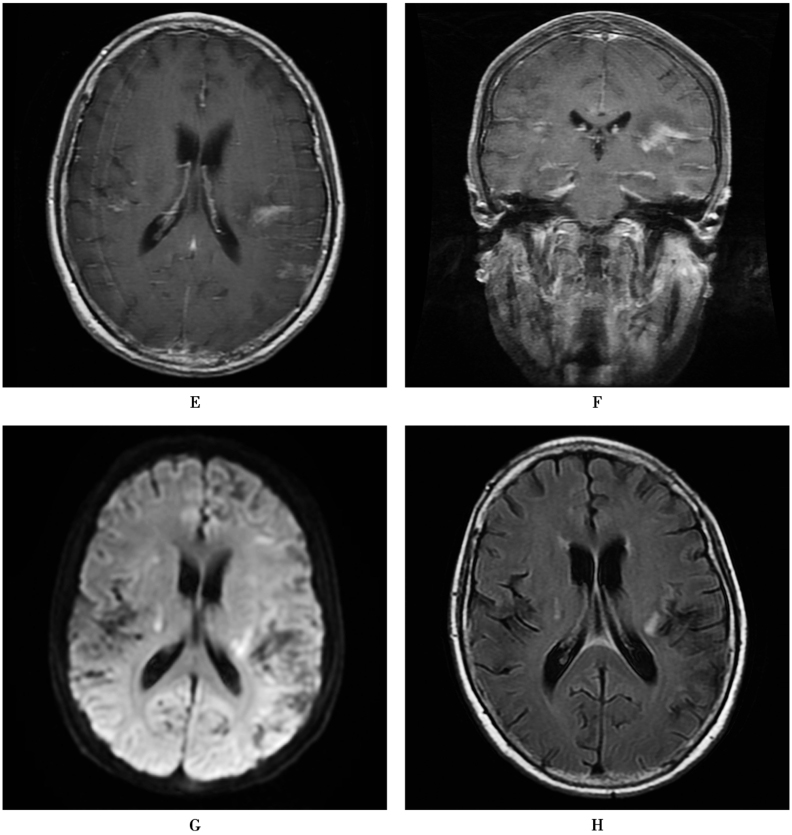
图10 脑膜血管型神经梅毒
患者,女,56岁,麻痹性痴呆。梅毒特异性抗体TPPA(+),梅毒荧光抗体IgG吸附试验FTA-ABS IgG(+),梅毒螺旋抗体TP-ab(+)。T2WI(A)、FLAIR(B)显示左侧额颞叶皮层、右侧额叶、右基底节多发高信号,大片状、斑片状;T1WI(C)上左侧额颞叶病变呈高信号,T2WI(D)上低信号,另见皮层下多发低信号,提示慢性出血;增强扫描(E、F)部分病变呈斑片状强化,强化灶位置较表浅;DWI(G)上脑内多发点、片状高信号;抗梅毒治疗20天后复查(H),病灶明显吸收减少
弓形体脑炎是艾滋病患者最常见的机会性感染,病变好发部位为基底节、背侧丘脑、额顶叶皮层下,也可见于脑干和小脑。以基底节区多见,可单发或多发。CT显示病灶呈环形和结节状强化,以环形强化为多见,中心为低密度。强化壁通常薄而均匀,较大的病灶也可厚而不规则。T2WI上病灶可以呈高信号(与脑实质比较),与周围水肿带不易区分;也可呈等信号或低信号,周围环绕高信号的水肿带。T1WI上病灶呈等或低信号。增强扫描显示病灶呈结节或环形强化,强化形式与CT增强相似。弓形体也是胎儿宫内先天感染的常见原因,影像学表现与后天的感染不同,多以脑积水、脑内多发点状钙化为特点;后天感染多以病灶周围大小不一、水肿带伴单发或多发环形强化为特点。艾滋病容易合并淋巴瘤,部分淋巴瘤可呈环形强化,与弓形体感染难以鉴别。MRS、灌注等技术对于鉴别诊断有一定的帮助。弓形体感染病灶内脂峰和乳酸峰明显升高,而其他代谢峰消失。淋巴瘤则表现脂峰和乳酸峰轻中度升高,胆碱峰明显升高,其他代谢峰减低但可见。灌注检查淋巴瘤为高代谢,弓形体感染为低代谢。
3.进行性多灶性白质脑病
是由于人乳头多瘤空泡病毒(JC病毒)感染所致,JC病毒见于80%的正常人体内,在免疫功能低下时可被激活。多见于艾滋病或其他免疫功能低下或接受免疫调节治疗的患者。疾病早期CT多无阳性发现。异常表现为脑白质内多发低密度灶,无占位效应,多无强化。病灶可同时累及双侧脑室周围和皮层下白质,也可单独累及一侧脑室旁或皮层下白质。MRI发现病灶的敏感度比 CT高,是PML首选检查方法。T2WI、FLAIR显示脑室周围或皮层下白质高信号,具有多灶性特点,可位于单侧,但以不对称双侧受累为多见,一般无占位效应,无强化,偶可见淡片状强化。脑皮层下病变位于灰白质交界处,由于侵犯皮层下U形纤维而呈扇形改变。T1WI上病灶呈低信号,边界都是多较清楚(图11)。进行性多灶性白质脑病多侵犯额叶、顶枕叶常见。约1/3病例可累及后颅窝,约10%病例仅表现为幕下病变。
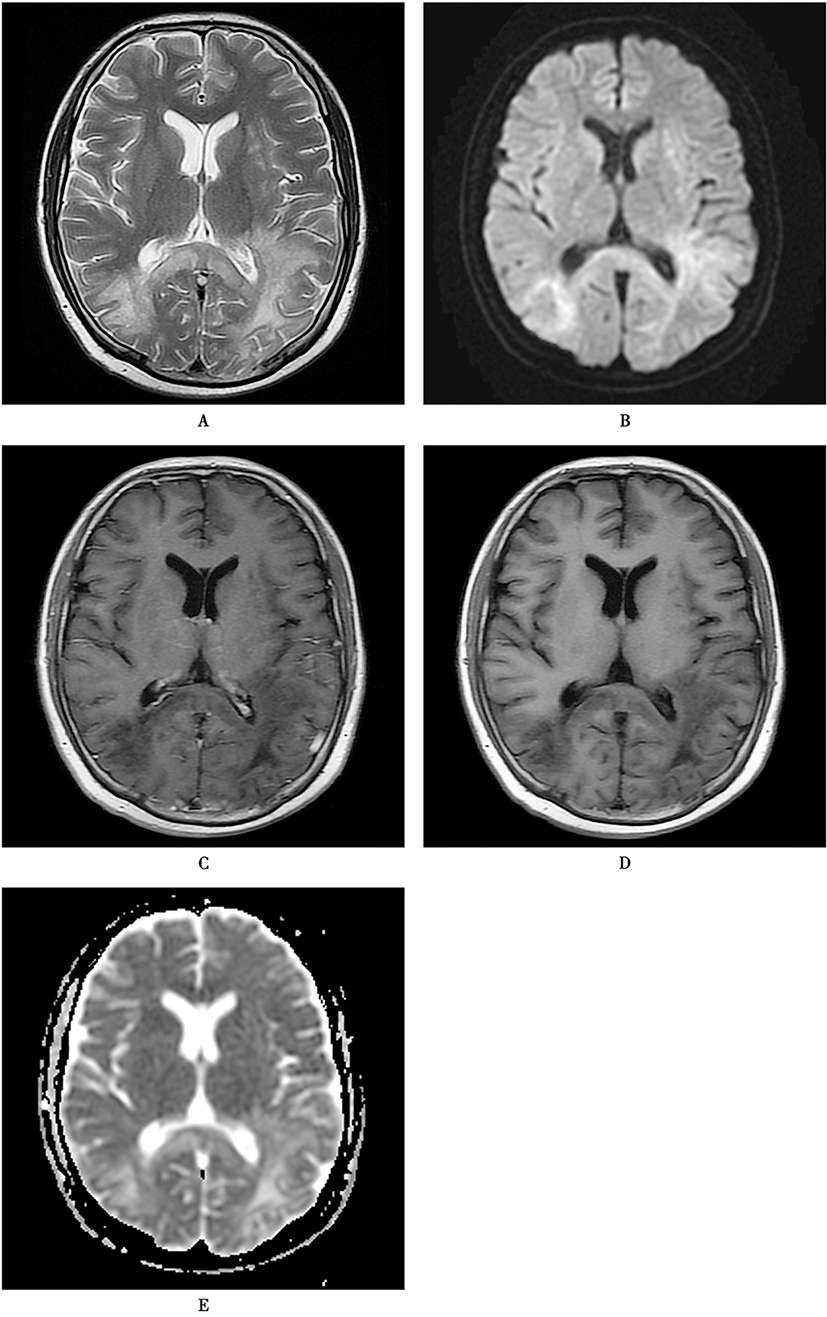
图11 进行性多灶性白质脑病
患者,女,30岁,右眼视物模糊2个月,言语不清1个月,加重半个月。血常规检查:白细胞6.24×109/L,淋巴细胞 0.78×109/L。 感染4项检查如下:HIV抗体初筛阳性, HIV病毒载量未归, T 细胞亚群(LY 371/μl,T 188/μl, T4,31/μl ,T8 131/μl,T4/T8 0.24)。 脑脊液人乳头多瘤空泡病毒 (JCV)DNA 20000拷贝/ml。 MRI双侧枕顶叶白质大片异常信号,T1WI(A)上低信号,T2WI(B)上高信号,DWI(C)上高信号, ADC(D)高,增强(E)无强化;病变累及胼胝体和皮层下U形纤维,无占位效应
男,医学博士,主任医师,教授。1970年出生于山东省茌平县。特长为神经系统影像诊断。擅长脑血管病、脑肿瘤、脑炎性病变、脑白质病、鞍区病变等临床常见疾病的影像诊断和鉴别诊断。对于神经系统疑难病变的诊断分析具有较丰富的经验。研究领域为神经影像新技术新方法。在国内率先开展了针对颅内动脉管壁结构的成像技术研究。该技术对于颅内动脉狭窄的病因分析,脑卒中发作的危险性评估,早期发现病变,指导临床干预具有重要价值。
免责声明
内容来源于人卫知识数字服务体系、人卫inside知识库,其观点不反映优医迈或默沙东观点。此服务由优医迈与胤迈医药科技(上海)有限公司授权共同提供。
如需转载,请前往用户反馈页面提交说明:https://www.uemeds.cn/personal/feedback
人卫知识数字服务体系





 Copyright © 2023 Merck & Co., Inc., Rahway, NJ, USA and its affiliates. All rights reserved.
Copyright © 2023 Merck & Co., Inc., Rahway, NJ, USA and its affiliates. All rights reserved.