与新型冠状病毒(2019-nCoV)对峙,除了抗疫一线这一主战场外,还有另外一个重要的战场——知识战场,即我们的学者争分夺秒地揭秘这一与我们初次谋面的疾病,并将之整理成指南或者专家共识,尽快将知识武器交到一线抗疫人员的手中,让其做到有的放矢箭无虚发。
北京大学第三医院药剂科受中国药学会和国际药师联合会委托,积极组织相关专家和药师,在对新型冠状病毒感染相关背景,临床表现与诊断,治疗,医院药学防控策略,医院药学工作指导,关键药品、设施和设备保障,特殊情况下药品的管理与使用等方面的相关资料进行分析、研判、总结的基础上,组织编写了中国《新型冠状病毒感染:医院药学工作指导与防控策略专家共识(第一版)》。
该共识已于2月6日在中国药学会网站进行发布,并于2月7日在中国知网(CNKI)由《中国药学杂志》在线发布。
应国际药学联合会(FIP)要求,该共识的英文版本已于2月7日在全球进行发布,为世界范围内抗疫工作的药学保障与服务提供了“中国经验”。
以下为中文版指南全文:
新型冠状病毒感染:医院药学工作指导与防控策略专家共识(第一版)
本文旨在为药学部门工作人员提供有关新型冠状病毒感染防控的相关信息和具体工作指导。
1 新型冠状病毒感染相关背景
1.1 流行病学特点
2019 年 12 月以来,新型冠状病毒感染在中国武汉暴发。世界卫生组织(WHO)1 月 12 日将这种致病病毒命名为 2019-nCoV。根据 WHO 应急委员会的建议,WHO 宣布将 2019-nCoV 疫情列为国际关注的突发公共卫生事件。截止 2020 年2 月 6 日,2019-nCoV 在全球已造成 28120 例患者感染,564 人死亡。
目前所见传染源主要是新型冠状病毒感染的肺炎患者,无症状感染者也可能成为传染源。经呼吸道飞沫和接触传播是主要的传播途径,气溶胶和消化道等传播途径尚待明确。人群对 2019-nCoV 普遍易感[1-3]。
1.2 病原学特点
新型冠状病毒属于β属的新型冠状病毒,有包膜,颗粒呈圆形或椭圆形,常为多形性,直径 60-140nm。其基因特征与 SARSr-CoV 和 MERSr-CoV 有明显区别[1,4]。目前研究显示,新型冠状病毒与蝙蝠病毒 TG13 的全基因组序列一致性高达 96%[5]。
2 临床表现与诊断
2.1 临床表现[1]
1) 发热和/或呼吸道症状;
2)具有肺炎影像学特征:早期呈现多发小斑片影及间质改变,以肺外带明显。进而发展为双肺多发磨玻璃影、浸润影,严重者可出现肺实变,胸腔积液少见;
3)发病早期白细胞总数正常或降低,或淋巴细胞计数减少。
其他症状包括咯血、肌肉疼痛、头痛、意识模糊、胸痛和腹泻等[6,7]。
2.2 临床诊断[1]
湖北省及湖北以外省份诊断略有差异。
2.2.1 疑似病例
流行病学史:
1) 发病前 14 天内有武汉市及周边地区,或其他有病例报告社区的旅行史或居住史;
2)发病前 14 天内与新型冠状病毒感染者(核酸检测阳性者)有接触史;
3)发病前 14 天内曾接触过来自武汉市及周边地区,或来自有病例报告社区的发热或有呼吸道症状的患者;
4)聚集性发病。
湖北以外省份有流行病学史中第 1~3 条的任何一条,符合临床表现中的 1~3条的任意 2 条;无明确流行病学史的,符合临床表现中的 1~3 条。
湖北省内有有流行病学史中的任何一条或无流行病学史,且符合临床表现中2 条。
2.2.2 临床诊断病例(限湖北省)
疑似病例具有肺炎影像学特征者。
2.2.3 确诊病例
疑似病例,具备以下病原学证据之一者为确诊病例:
1) 呼吸道标本或血液标本实时荧光 RT-PCR 检测新型冠状病毒核酸阳性;
2) 呼吸道标本或血液标本病毒基因测序,与已知的新型冠状病毒高度同源。
2.3 临床分型[1]
2.3.1 轻型
临床症状轻微,影像学未见肺炎表现。
2.3.2 普通型
具有发热、呼吸道等症状,影像学可见肺炎表现。
2.3.3 重型
符合下列任何一条:
1) 呼吸窘迫,RR≥30 次/分;
2)静息状态下,指氧饱和度≤93%;
3)动脉血氧分压(PaO2)/吸氧浓度(FiO2)≤300mmHg(1mmHg=0.133kPa);
2.3.4 危重型
符合以下情况之一者:
1) 出现呼吸衰竭,且需要机械通气;
2) 出现休克;
合并其他器官功能衰竭需 ICU 监护治疗。
3 治疗
3.1 治疗药物特点与注意事项
新型冠状病毒目前尚无确认有效的针对性治疗药物。以下药物可在临床试用或处于临床研究阶段。由于相关疾病治疗研究还在进行,建议及时关注最新研究证据。
3.1.1 干扰素[1]
可试用 α-干扰素雾化吸入,成人每次 500 万 IU,加入灭菌注射用水 2mL,每日 2 次。常见不良反应包括发热、疲劳、头痛、关节痛、食欲不振等。注意对有抗生素过敏史的患者应谨慎使用,初次用药过程中应严密监测。雾化过程中应注意避免接触眼睛。保存及运输过程中注意 2-8℃避光保存。在特殊情况下使用注射液进行雾化时,应注意超适应证的风险问题。
3.1.2 洛匹那韦/利托那韦[1]
洛匹那韦/利托那韦胶囊:200mg/50mg 每粒,每次 2 粒,每日 2 次,口服给药。使用时应注意整片吞咽,不能咀嚼、掰开或压碎。可与食物同服。
洛匹那韦/利托那韦口服液:80mg/20mg 每毫升,每次 5 mL,每日 2 次。必须与食物同服,可以进行管饲给药。辅料中含有乙醇与丙二醇。
轻中度肝功能不全、肾功能不全及行替代治疗患者无需调整剂量。重度肝功能不全患者不建议使用。常见不良反应包括腹泻、恶心呕吐、高甘油三酯血症、上呼吸道感染、肝功能损害等。同时应注意与其他药物的相互作用问题。
3.1.3 利巴韦林[1]
参照国家卫生健康委员会诊疗方案(试行第五版),抗病毒治疗可加用利巴韦林,成人 8 mg/kg iv 每 8 小时一次。有严重贫血、肝功能异常者慎用。老年人不推荐应用。可透过胎盘与乳汁,有生殖毒性,停药 4 周尚不能完全从体内清除。在 SARS 和 MERS 期间有过大剂量利巴韦林的临床应用经验,但也发现大剂量使用时可能出现与剂量相关的贫血,可能在用药后 3-5 天出现,存在基础心脏疾病患者可能出现因贫血导致的心功能恶化。此外也有低电解质紊乱与中枢神经系统毒性的报道,故临床应用需谨慎[8,9]。
3.1.4 抗菌药物
避免盲目或不恰当使用抗菌药物[1]。
根据 WHO 指南建议[10],建议给予经验性抗菌药物,对于考虑脓毒症的患者,应在初次评估 1 小时内给予经验性抗菌治疗。使用过程中注意输注速度与配置后可放置时间,观察可能出现的过敏反应如皮疹等;口服制剂应注意与微生态制剂等间隔 2 小时服用。
3.1.5 糖皮质激素
不应常规使用[1,10]。可根据患者呼吸困难程度、胸部影像学进展情况,酌情短期内(3~5 天)使用糖皮质激素,建议每天剂量不超过相当于甲泼尼龙 1~2mg/kg[1,6]。使用过程中应监测血糖、电解质,可能出现中枢兴奋症状,常见如失眠等,可对症处理。
3.1.6 对症支持治疗
可对症使用解热镇痛、镇咳、化痰、止吐、缓泻剂、解痉、肠道微生态调节剂等药物。
3.1.7 藿香正气胶囊(丸、水、口服液)[1,11]
功能为解表化湿,理气和中。口服。软胶囊:一次 2-4 粒,一日 2 次;滴丸:一次 2.6g,一日 2 次;水、口服液:5~10mL,一日 2 次,用时摇匀。文献报道不良反应有引起药疹、紫癜、休克等过敏反应及肠梗阻、上消化道出血、过敏性哮喘、酒醉貌样过敏、过敏性休克,外用引起肠梗阻、小儿低血糖、小儿抽搐、双硫仑样反应。风热感冒者慎用。孕妇慎用。有高血压、心脏病、肝病、糖尿病、肾病等慢性病严重者应谨慎使用。
藿香正气水因含酒精,酒精过敏者禁用。服药后不得驾驶机、车、船、从事高空作业、机械作业及操作精密仪器,不可与替硝唑、甲硝唑等药物合并使用[12]。
3.1.8 金花清感颗粒[1]
功能为疏风宣肺,清热解毒。用开水冲服。一次 1 袋,一日 3 次,疗程 3天。
常见不良反应包括恶心、呕吐等胃肠道不良反应,偶见用药后肝功能异常,心悸或皮疹。对本品过敏者禁用。运动员及脾胃虚寒者慎用,既往有肝脏病史或服药前肝功能异常者慎用,孕妇、哺乳期妇女,儿童及老龄人群谨慎使用。成分中的麻黄可升高血压,因此高血压患者慎用,同时服药时需监测血压[13]。服药期间不宜同时服用滋补性中药。
3.1.9 连花清瘟胶囊(颗粒)[1,11]
功能为清瘟解毒,宣肺泄热。口服。胶囊:一次 4 粒,一日 3 次;颗粒:一次 1 袋,一日 3 次。
文献报道[1,11] 该药可能易导致消化系统不良反应,也可导致皮疹、瘙痒等皮肤及附件损害。风寒感冒者不适用。成分中的麻黄可升高血压,因此高血压、心脏病患者慎用。有肝病、糖尿病、肾病等慢性病严重者,儿童、孕妇、哺乳期妇女、年老体弱及脾虚便溏者谨慎使用。对本品过敏者禁用。过敏体质者及运动员慎用。本品不宜长期服用。
需置阴凉干燥处(不超过 20℃)保存。
3.1.10 疏风解毒胶囊[1]
功能为疏风清热,解毒利咽。口服。胶囊:一次 4 粒,一日 3 次。
偶见恶心的不良反应。过敏体质及对本品过敏者禁用。结膜热、疱疹性咽峡炎、妊娠及哺乳期妇女谨慎使用。
3.1.11 防风通圣颗粒[1,11]
功能为解表通里,清热解毒。口服。一次 1 袋,一日 2 次。不良反应偶见胃肠道反应、皮疹、痛痒等。脾虚便溏者忌用。成分中的麻黄可升高血压,因此高血压、心脏病患者慎用。肝病、糖尿病、肾病等谨慎服用。孕妇,运动员,儿童、哺乳期妇女、年老体弱、过敏体质者慎用。对本品过敏者禁用。
3.1.12 喜炎平注射液[1]
功能为清热解毒,止咳止痢。肌内注射:成人一次 50~100mg,一日 2-3 次;
小儿酌减或遵医嘱;静脉滴注:一日 250~500mg,加入 5%葡萄糖注射液或 0.9%氯化钠注射液稀释后静脉滴注;或遵医嘱。儿童:一日按体重 5~10mg/kg(0.2~0.4ml/kg),最高剂量不超过 250mg,以 5%葡萄糖注射液或 0.9%氯化钠注射液 100ml~250ml 稀释后静脉滴注,控制滴速每分钟 30~40 滴,一日 1 次。
偶见皮疹、瘙痒、发热、寒战、疼痛、烦躁,罕见呼吸急促、紫绀、心悸、抽搐等不良反应。对该药过敏者、孕妇禁用。有药物过敏史者、老人、婴儿等特殊人群应慎用,初次使用的患者应加强监测。严格控制输液速度,儿童以 30~40滴/分钟为宜,成人以 30~60 滴/分钟为宜。置阴凉处(不超过 20℃)保存。
3.1.13 血必净注射液[1]
功能为化瘀解毒。静脉输注 100mL/日,每日 2 次。不良反应偶见皮肤瘙痒。对本品过敏者、中高龄患者应谨慎使用[16],孕妇禁用。不超过 20℃干燥保存。
3.1.14 参附注射液[1,11]
功能为回阳救逆,益气固脱。肌内注射:一次 2~4mL,一日 1-2 次;静脉滴注;每次 20-100mL,用 5%葡萄糖注射液稀释至 250mL 或 500mL;静脉推注;每次 5~20mL,用 5%葡萄糖注射液 20mL稀释后使用,伴有糖尿病等特殊情况时,可用 0.9%氯化钠注射液稀释后使用,配置后 4 小时内使用,连续使用不宜超过20 天。主要不良反应为过敏反应,包括皮疹、急性哮喘发作、过敏性胃肠炎、眼睑水肿、过敏性休克[1,11],并可导致肝功能异常,频发房性早搏、心电图异常、头痛、面色潮红、恶心、高血压患者血压升高等。孕妇禁用。过敏体质者慎用。本品有小毒,不宜长期使用。不宜与中药半夏、瓜蒌、贝母、白蔹、白及、五灵脂、藜芦等同时使用。
3.1.15 生脉注射液[1,11]
功能为益气养阴,复脉固脱。肌内注射:一次 2~4mL,一日 1~2 次;静脉滴注:一次 20~60mL,用 5%葡萄糖注射液 250~500mL 稀释。其不良反应以速发型过敏反应为主,主要表现为皮肤过敏反应,过敏性休克,尚可导致严重腹胀、角膜水肿等。孕妇禁用。过敏体质者慎用。年老体弱者、心肺严重疾患者、肝肾功能异常者和初次使用中药注射剂的患者要加强临床监护。不超过 20℃保存。
3.2 药学监护
各医疗机构药师应结合当地实际情况,积极参与到患者的药物治疗中,在审
方、调配、安全性监测或药物重整等环节中关注可能出现的药物相互作用、不良反应和重复用药等风险,为临床安全、合理、有效用药保驾护航。
3.2.1 药物相互作用
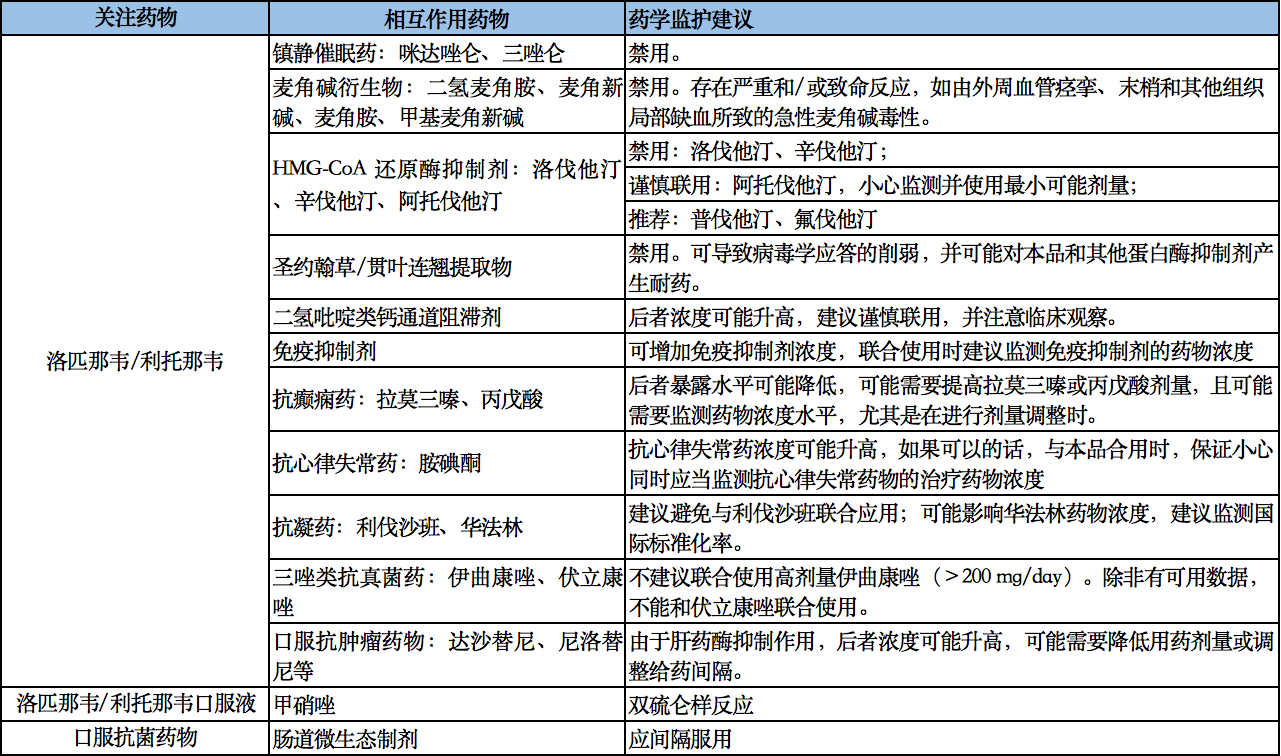
关于可能出现的药物相互作用,包括药物吸收、分布、代谢、排泄等各个环节可能出现的对治疗产生影响的相互作用。避免将经 CYP3A4 代谢的药物与洛匹那韦/利托那韦联合使用。避免将口服抗菌药物与微生态制剂联合使用。
表 3.1 值得关注的药物-药物相互作用及药学监护建议列表
3.2.2 不良反应
药师应当关注所用药物的不良反应,尤其是临床试用药物与临床研究药物的不良反应。注意与疾病症状相鉴别,鉴别方法包括药物不良反应的因果关联判断,药物使用时间相关性等。药师可结合所在医疗机构实际情况,进行不良反应的上报、主动监测与临床预警,有条件情况下积极关注出院患者用药情况、ADR情况、预后情况等,及时将药品安全性信息进行分析,反馈临床,及时调整治疗方案,保障临床用药安全。
3.2.3 重复用药
关注重复用药风险,如不同复方解热镇痛药中含有相同成分,易发生因重复用药引起的肝肾功能损伤等情况。在处方调配、远程用药指导、或用药重整等过程中,建议梳理患者所有使用药物,尤其是复方制剂,对药物治疗方案提出合理化建议。
3.2.4 妊娠患者
孕产妇感染新型冠状病毒在各孕龄均有可能发生[18,19]。且妊娠期妇女对病毒性呼吸系统感染的炎症应激反应明显增高,病情发展迅速,尤其是中晚期妊娠,易发展为重症,需住院密切观察,隔离收治,由感染科、产科、ICU 等相关科室共同管理[18,19]。对于疑似或确诊新型冠状病毒的孕妇接受推荐方案治疗时,需要考虑妊娠的生理性因素[10],建议使用 FDA 妊娠安全分级 B、C 类药物,尽量避免使用 D 类药物。在使用探索性治疗方案时,需要咨询产科专家和伦理委员会,基于母亲的潜在获益和胎儿的安全,进行个体化的利弊分析与评估[10]。紧急分娩和终止妊娠的决定基于多个因素,包括孕龄、母亲的状况、胎儿的稳定性等。必须咨询产科、新生儿科和 ICU 的专家,并视母亲情况进行处置[10]。
3.2.5 新生儿
截止至 2 月 5 日,武汉出现了一例母亲感染新冠病毒肺炎的新生儿,出生30 小时后咽拭子新冠病毒核酸检测阳性,胸片提示有肺部感染。新型冠状病毒是否通过母婴垂直传播目前尚不明确。母亲感染新型冠状病毒的新生儿应在负压病房中监护,考虑有感染风险,出生后建议隔离 10~14 天。产妇未愈前,不建议母乳喂养,以防止新型冠状病毒的传播[20]。
3.2.6 儿童及青少年
抗病毒药物的效果和在儿童中应用的安全性未知,对危重症患儿可参考成人的用药选择,轻症可选用干扰素雾化。避免盲目或不恰当使用抗菌药物。除非特殊原因,应避免常规使用糖皮质激素[21]。
3.2.7 老年人
老年人免疫功能减弱,且多合并慢性基础疾病,感染后病情较重,目前据报道死亡患者多为老年人合并有基础疾病者。根据基础疾病的不同,按时、规律、规范服用药物,做好相关疾病的二级预防治疗。同时根据患者的肝、肾功能进行用药剂量的调整,并密切关注药物之间的相互作用。
3.2.8 营养支持治疗
住院患者入院时根据 NRS2002 评分进行营养风险筛查。NRS2002 总评分≥3分时,应尽早给予营养支持疗法[22]。
对于无法经口进食的重症患者,可放置鼻胃管或鼻空肠管,应用重力滴注或肠内营养输注泵泵入营养液[23]。对于存在严重胃肠道功能障碍的患者,需采用肠外营养以维持基本营养需求[24]。
根据美国肠外肠内营养学会(ASPEN)成人营养支持指南,推荐病情稳定患者每日摄入蛋白质 0.8~1.5 g/kg/d,总热量 20~30 kcal/kg/d;推荐重症患者或脓毒症患者每日摄入蛋白质 1.2~2.5 g/kg/d,总热量 20~30 kcal/kg/d[25,26]。在营养支持的早期阶段,推荐允许性低热卡方案,即达到目标摄入量的 60%~80%;待病情减轻后,逐步补充能量与营养素,直至达到目标摄入量。在病情逐渐缓解的过程中,可摄入半流质、易于咀嚼和消化的食物。少量多餐,每日 5~6 餐,补充足量优质蛋白质。随病情好转,逐步向普通饮食过渡。
3.2.9 中药注射剂
中药注射剂禁止与其他注射剂配伍使用。输注本品前后,应用适量稀释液对输液管道进行冲洗。在输液的过程中,要仔细观察,滴速宜慢,静滴初始 30 分钟内应加强监护,发现不良反应,应及时停药。
3.2.10 中成药饮食禁忌
服药期间忌烟、酒及辛辣、油腻、鱼虾、海鲜类食物。清热解毒类药物服用期间不宜与补益类的药物同时服用。
3.3 传统医学(中医)治疗[1]
本病属于中医疫病范畴,病因是感受疫戾之气,各地可根据病情、当地气候特点以及不同体质等情况,参照下列方案进行辨证论治。
3.3.1 医学观察期
临床表现 1:乏力伴胃肠不适
推荐中成药:藿香正气胶囊(丸、水、口服液)
临床表现 2:乏力伴发热
推荐中成药:金花清感颗粒、连花清瘟胶囊(颗粒)、 疏风解毒胶囊(颗粒)、防风通圣丸(颗粒)
3.3.2 临床治疗期
1)初期:寒湿郁肺 临床表现:恶寒发热或无热,干咳,咽干,倦怠乏力,胸闷,脘痞,或呕恶,便溏。舌质淡或淡红,苔白腻,脉濡。
推荐处方:苍术 15g、陈皮 10g、厚朴 10g、广藿香 10g、 草果 6g、麻黄6g、羌活 10g、生姜 10g、槟榔 10g
2)中期:疫毒闭肺 临床表现:身热不退或往来寒热,咳嗽痰少,或有黄痰,腹胀便秘。胸闷气促,咳嗽喘憋,动则气喘。舌质红,苔黄腻或黄燥,脉滑数。
推荐处方:苦杏仁 10g、生石膏 30g(先煎)、瓜蒌 30g、生大黄 6g(后下)、生、炙麻黄各 6g、葶苈子 10g(包煎)、桃仁 10g、草果 6g、槟榔 10g、苍术 10g
3)重症期:内闭外脱 临床表现:呼吸困难、动辄气喘或需要辅助通气,伴神昏,烦躁,汗出肢冷,舌质紫暗,苔厚腻或燥,脉浮大无根。
推荐处方:人参 15g、黑顺片 10g(先煎)、山茱萸 15g,送服苏合香丸或安宫牛黄丸
推荐中成药:血必净注射液、参附注射液、生脉注射液
4)恢复期:肺脾气虚 临床表现:气短、倦怠乏力、纳差呕恶、痞满,大便无力,便溏不爽,舌淡胖,苔白腻。
推荐处方:法半夏 9g、陈皮 10g、党参 15g、炙黄芪 30g、 茯苓 15g、藿香 10g、砂仁 6g(后下)
4 医院药学防控策略
4.1 制定应急预案和工作流程
为保障疫情期间药学部门感染预防与控制工作的有效实施,并提供有效药学服务保障,应在医疗机构统一领导下,成立药学工作领导小组,建立相应的应急预案和工作流程。其内容可包括但不限于:人力资源管理、药品保障供应、药品调剂管理、临床药学服务管理、用药咨询管理、药品质量控制管理、药学教育与科研管理、疫情防控与消毒、捐赠药品管理和有关信息上报等[27]。
4.2 开展全员培训
应对全员进行 2019-nCoV 防控知识的培训,并依据岗位职责确定针对不同人员的培训内容,尤其是对高风险的部门(发热药房、隔离病区的药房、急诊药房)和参加高风险操作(如有与确诊或疑似患者的接触、患者标本处理可能产生的气溶胶或体液暴露的接触操作)的药学人员要重点培训。可利用多种方式提高培训效率和效果,如现场培训联合网络继续教育培训,督促成员及时完成学习培训,确保其熟练掌握新型冠状病毒感染的防控知识、方法与技能,做到有效防控、早发现、早报告、早隔离、早诊断、早治疗、早控制[28]。
4.3 关注药师健康[28-30]
药学部门应当合理调配人力资源和班次安排,避免药师过度劳累,注意合理饮食。
针对岗位特点和风险评估结果,开展主动健康监测,包括体温和呼吸系统症状等。采取多种措施,保障药师健康地为患者提供医疗服务。
应关注药师的心理健康及情绪管理。必要时评估药师的心理状况,根据指南及原则对有需要的药师进行心理疏导(可访问北京大学第六医院(北京大学精神卫生研究所)网站:http://www.pkuh6.cn/)。
4.4 做好药学人员防护
药学部门应当规范消毒、隔离和防护工作,储备质量合格、数量充足的防护物资,如消毒产品和医用外科口罩、医用防护口罩、隔离衣、眼罩等防护用品,确保药学部门工作人员防护到位。
在严格落实标准预防的基础上,强化接触传播、飞沫传播和空气传播的感染防控。正确选择和佩戴口罩,手卫生是感染防控的关键措施[28]。新型冠状病毒感染流行期间,药学部门工作人员根据不同工作岗位和需要执行的操作及不同的暴露风险,可依据国家卫生健康委员会发布的指南[31]和其他指南[32]进行安全防护。
4.5 加强药师感染监测[28,33]
应加强药师对感染防控工作早期的自我预警及预报意识。发现疑似新型冠状病毒感染的药师时,应当按照有关要求及时报告,并在 2 小时内上报信息,做好相应处置工作。
对高风险部门(发热药房、隔离病区的药房、急诊药房)工作的药师和参加高风险操作(如有与确诊或疑似患者的接触、患者标本处理可能产生的气溶胶或体液暴露的接触操作)的药师进行重点监测。
4.6 做好清洁消毒管理[1,33-37]
因新型冠状病毒可通过飞沫及接触传播,应对医院药学部门相应区域进行环境消毒。既往 SARS-CoV 和 MERS-CoV 研究结果显示:病毒对紫外线和热敏感,56℃ 30 分钟、乙醚、75%乙醇、含氯消毒剂、过氧乙酸和氯仿等脂溶剂均可有效灭活病毒,氯己定不能有效灭活病毒。
药学部门应根据相关清洁消毒指南及规定,对工作环境、相关物品和设备,做好清洁消毒工作。
4.7 加强患者就诊管理[28]
应当做好就诊患者的管理,尽量减少患者的拥挤,以减少医疗机构感染的风险。对于现场接受药学服务的患者,应询问患者有无 2019-nCoV 感染相关症状及流行病学接触史,发现疑似或确诊感染 2019-nCoV 的患者时,应立即上报医疗机构相关部门并配合采取隔离或者控制传播措施。
4.8 加强患者教育[27]
药师应当积极通过药学门诊、窗口咨询等开展就诊患者及其陪同人员的教育,使其了解 2019-nCoV 的防护及用药知识,有条件的情况下可面向公众加强对2019-nCoV 预防和治疗药物的知识科普,并通过网络、电话等途径向自我医学观察人员提供药学服务。
4.9 加强感染暴露管理[37]
严格落实医疗机构感染预防与控制的各项规章制度,减少药学服务过程中潜在感染传播媒介(如纸质处方、药品运输工具等)的接触,最大限度降低感染暴露的风险。增强敏感性,若发生 2019-nCoV 感染暴露,应立即上报医疗机构相关部门,并依据相关标准和流程,启动应急预案,配合做好调查处置工作。
4.10 加强医疗废物管理[38]
将 2019-nCoV 感染确诊或疑似患者产生的医疗废物,纳入感染性医疗废物管理,应按卫生行政管理部门或医疗机构相关规定,分类收集药学服务过程中可能产生的医疗废物并配合相关部门进行规范处置,要做到专人管理、及时收集、做好记录、分类存放、专车运输、定点处置。
5 医院药学工作指导
5.1 药学工作岗位的感染暴露风险和管理[39]
药学工作人员的个人防护应严格按照所在医疗机构感染防控的要求进行。按标准预防原则,参考对应或类似临床医疗操作高、中、低三级暴露风险,根据药学工作岗位的特点进行评估,药学工作岗位大部分属于低风险,个别岗位属于中、高风险。
(1)高风险:发热或隔离病区的药房工作,并按照发热或隔离病区相关要求进行防护。如有与确诊或疑似患者的接触、患者标本处理可能产生的气溶胶或体液暴露的接触操作等。如药学实验室不具备生物安全二级实验室以上条件,不建议对确诊和疑似患者进行血药浓度测定和基因检测。
(2)中风险:直接接触患者,如:药学服务中的查体、患者体液(含血液)接触、转运及非确诊或疑似患者血药浓度测定和基因检测等。
(3)低风险:间接接触患者,如:处方调剂、用药咨询、药学门诊、药学监护、病区送药、静脉配置药物、药品管理等岗位。
5.2 常用防护用品和装备
常见的医用防护用品包括医用防护口罩、乳胶检查手套、护目镜、防护面罩/防护面屏、防水围裙、隔离衣、防护服等[31,39]。医务人员使用的防护用品应符合国家标准[31]。医用防护用品被患者血液、体液、分泌物等污染时应当立即更换,并应严格按照各自医疗机构感控部门要求进行个人和环境处理[28,40]。
5.3 不同岗位药学人员的个人防护措施[1,39,40]
(1)高风险:防护服、隔离衣、医用防护口罩、工作帽、护目镜/面屏、呼吸头罩、双层手套、防水靴套、鞋套、手卫生;
(2)中风险:工作服并加穿隔离衣、医用外科口罩/医用防护口罩、工作帽、护目镜/面屏、手套、手卫生;
(3)低风险:工作服或加穿隔离衣、医用外科口罩、工作帽、手卫生。
穿脱个人防护措施时应严格按照穿脱流程进行,禁止穿着个人防护装备离开污染区,以避免各个分区交叉感染。
5.4 工作设施和环境的管理[1,40]
5.4.1 工作设施管理
运送设备和容器:隔离区与非隔离区的药品运送设备和容器不能混用,运送设备和容器按所处环境的要求进行消毒。
处方:发热药房和隔离区药房应尽量使用电子处方,或采用信息手段传递处方(如传真、网络等),最大限度减少纸质处方的传递。纸质处方应定期集中汇总,经甲醛熏蒸消毒和环氧乙烷灭菌后,装入密封容器内保存。医院或药学部门应设置专门区域存放消毒后的处方。
5.4.2 环境管理
药学部门应进行药学部门环境消毒。药房应保持发药窗口清洁无杂物,疫情期间用 75%酒精、含有效氯 250mg/L~500mg/L 的含氯消毒剂或有效的消毒湿巾,每天两次对发药窗口进行擦拭消毒,每天四次对发热药房、传热病药房的发药窗口进行擦拭消毒。
5.5 接受药学服务的患者管理[28]
5.5.1 患者就诊和取药
药学部门应通过各种手段减少患者来医院就诊次数,例如根据各地医保情况允许开具长处方、提供网络咨询服务、药学部门使用物流直接配送药品到家等,减少患者不必要的就诊,降低交叉感染风险。
5.5.2 患者问诊
为患者直接提供药学服务的药师应注意患者体温,询问患者发热、呼吸道症状和流行病学史,如有疑似患者,应立即转诊至发热门诊。
5.5.3 药学服务
在疫情期间常规药学服务如果不能正常进行,可采取网络/电话/视频等形式线上进行。药师应加强针对疫情的药品的用药指导,注重不良反应观察和上报,避免药物相互作用,科学指导,促进合理用药。
5.5.4 患者教育
药师应积极开展就诊患者及其陪同人员的教育,使其了解新型冠状病毒的防护知识,指导其正确使用药物,避免过度的预防用药。疫情期间可通过非接触方式积极开展患者教育和用药咨询。
5.5.5 居家药学服务
药师可通过网上问诊APP为居家隔离和自我医学观察的人群进行用药指导,提供远程居家药学服务。
5.5.6 人文关怀
药学服务应传递人文关怀,通过各种形式,如用药交代或患者教育资料中增加鼓舞士气的文字,药师需要鼓励患者保持良好心态,战胜疫情。
6 关键药品、设施和设备保障
6.1 关键治疗药品清单和库存保障
针对新型冠状病毒感染疫情防控,医疗机构药学部门应保障临床诊疗相关的药品的供应。
关键治疗药品为用于医疗机构诊疗、疫情防控,以及医疗机构派出的医疗支援队所需的配备药品。由各医疗机构药事管理与药物治疗学委员会授权药学部门,根据临床诊疗进展和疫情防控需求,从药学专业角度制定关键治疗药品清单,参见表 6.1。
由药学部门指定人员负责关键治疗药品的采购、储存和发放,并根据诊疗方案、临床治疗需求、药品储备情况及时调整库存以保证临床使用需求。
表 6.1 新型冠状病毒感染的关键治疗药品参考清单
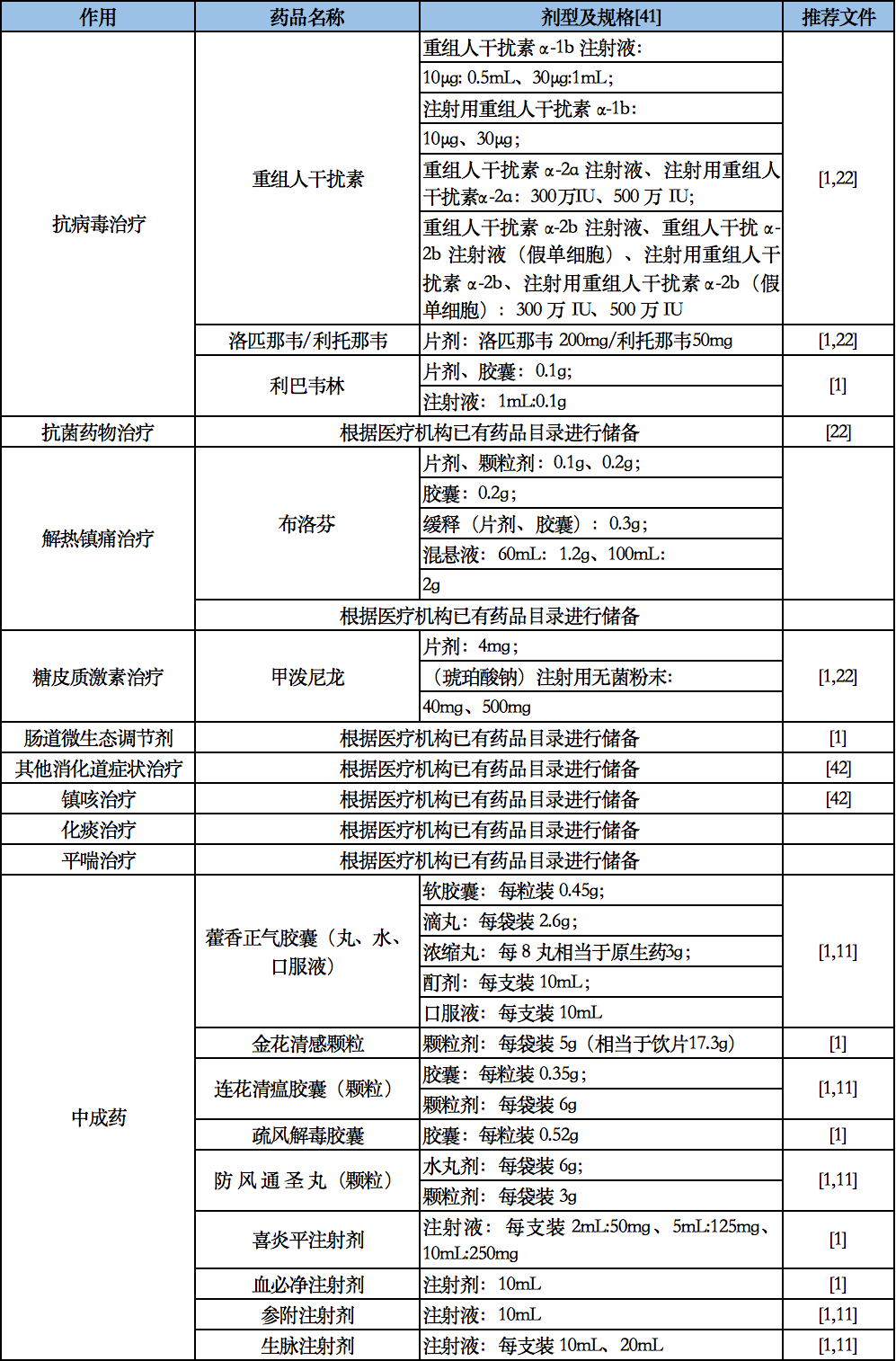
注:本药品清单所列药品仅供参考,各医疗机构可视具体情况调整。
6.2 消毒药品、消毒用耗材清单和库存保障
针对新型冠状病毒感染疫情防控,医疗机构药学部门与感染管理部门协商确定采购消毒药品清单,参见表 6.2,及时做好各部门消毒、防护工作。
药学部门也应对本部门物体表面、空气、手和处方等潜在污染对象进行定期消毒,将所需消毒药品、消毒用耗材情况上报医疗机构请领。
所有消毒药品、消毒用耗材应符合国家卫生健康部门管理要求。
表 6.2 新型冠状病毒感染常见污染对象的消毒药品、消毒用耗材参考清单[33,36,40]
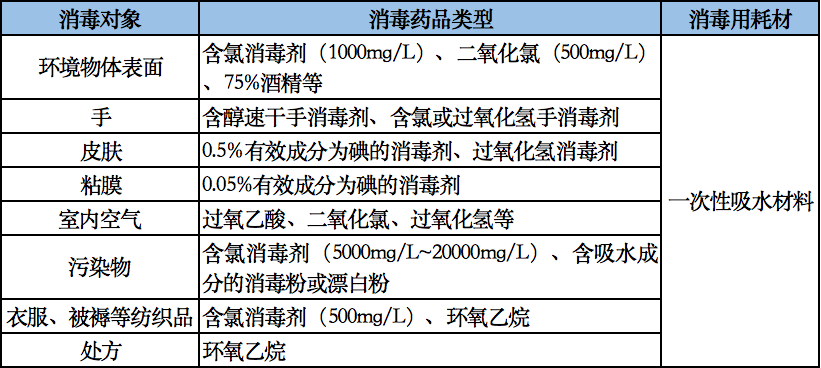
6.3 关键设施和设备的清单和管理
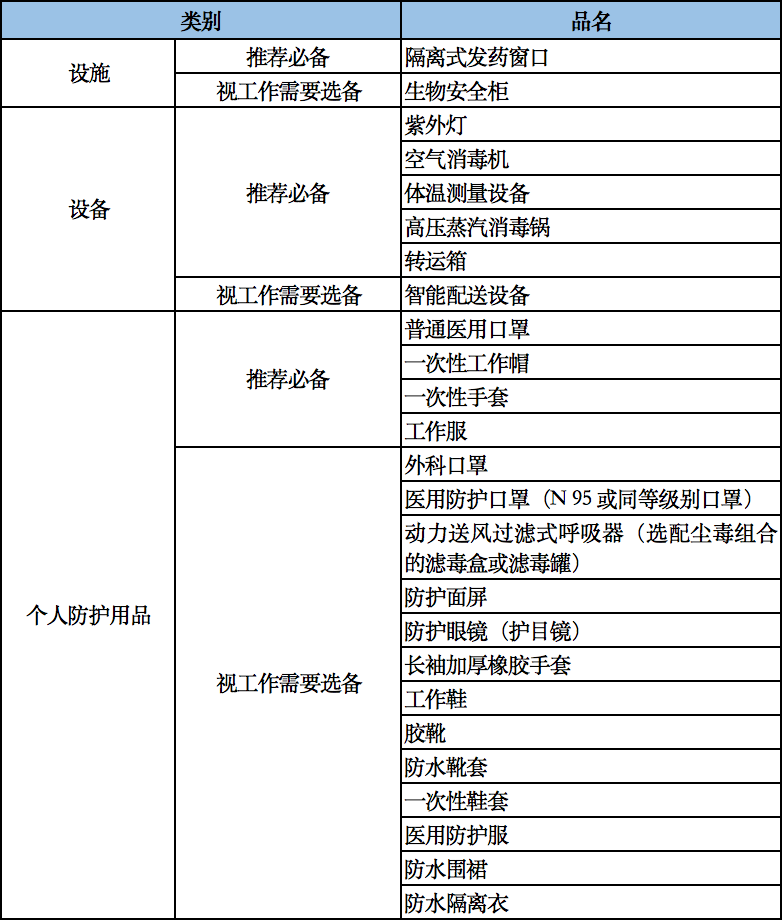
针对新型冠状病毒感染疫情防控,医疗机构药学部门制定疫情防控所需相关设备、设施和个人防护用品清单,参见表 6.3,相关设备应具备符合国家要求的合格证书,并保证由符合资质的人员按标准操作规程进行正常操作、运行和维护。个人防护用品应符合国家卫生健康部门管理要求。
表 6.3 新型冠状病毒感染疫情防控关键设施、设备和个人防护用品参考[31,36,40]
7 特殊情况下药品的管理与使用
7.1 捐赠药品管理与使用[40,43]
捐赠药品系指由相关供应商、生产厂家和其他组织自愿无偿向医疗机构提供的用于新型冠状病毒感染的肺炎预防、治疗与保健等相关药品。
捐赠药品应为医疗机构诊疗、疫情防控需要的药品,应符合国家食品药品监督管理和卫生行政等政府部门的规定,为合格的上市药品,其有效期应当在可执行的合理期限之内,还需通过医疗机构指定管理部门审批备案和资质审查。
在接受捐赠药品工作中,医疗机构应当遵守国家法律、法规的规定;在使用捐赠药品时,药学部门应严格按照医疗机构规定的流程和要求执行,不得私自接受、使用赠药,不得从事营利活动。设立专人、专库、专账管理捐赠药品,接受医疗机构指定管理部门的监督与审计。
7.2 临床试验用药品管理与使用[44,45]
针对新型冠状病毒感染疫情防控开展的相关临床试验,试验涉及药品的使用由主要研究者负责基于医学伦理原则使用,药学部门应配合研究者管理临床试验用药品。
试验用药品的剂量与用法应遵照试验方案,使用过程中应记录包括数量、装运、递送、接受、分配、应用后剩余药物回收与销毁等方面的信息。试验用药品的供给、使用、储藏及剩余药物的处理过程应符合国家相关规定。
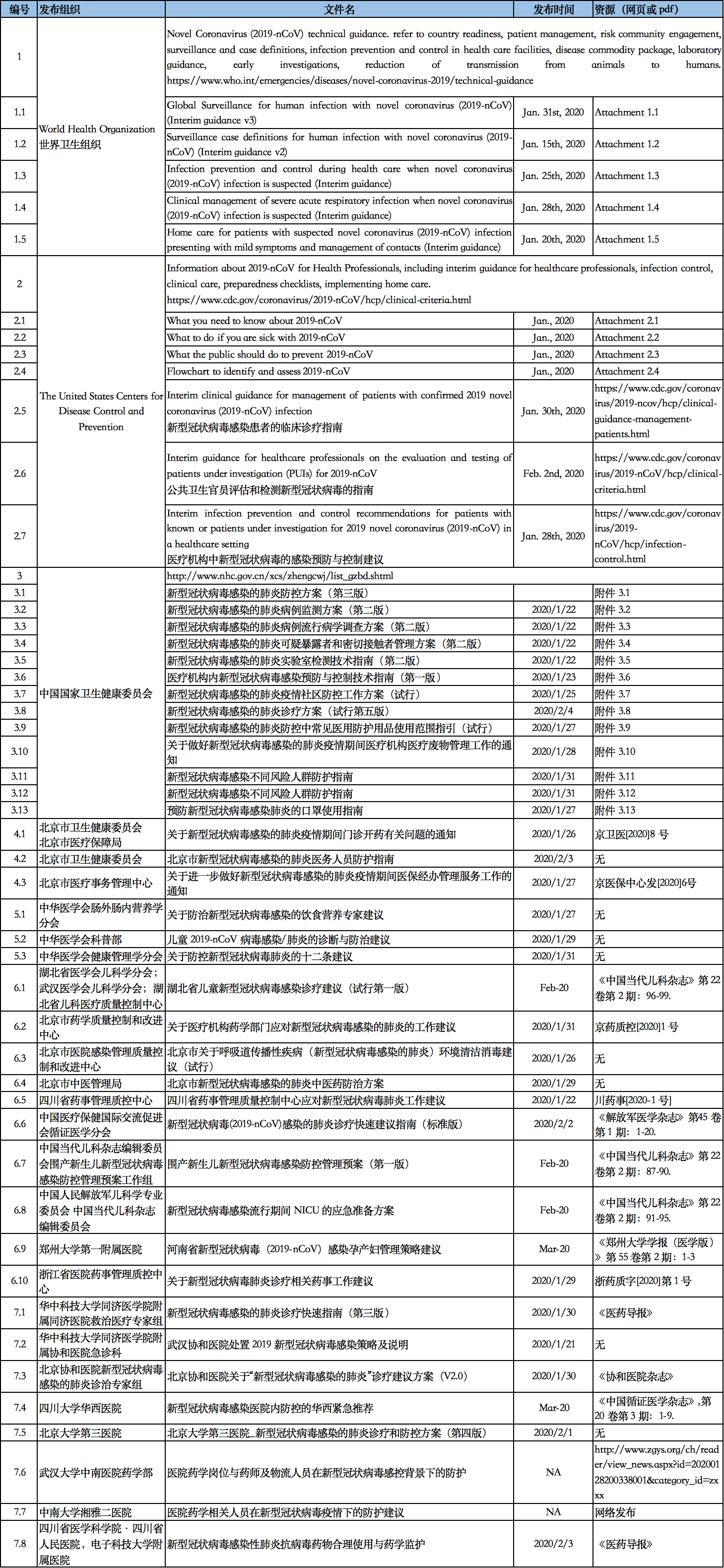
8 可靠的信息来源及其他相关资源
本文列示的相关信息资源为可以被检索到的相关资源。
参考文献
[1] 国家卫生健康委办公厅. 新型冠状病毒感染的肺炎防控方案(第五版)(国卫办医函[2020]103号)[EB/OL]. [2020-02-04].
[2] Li X, Zai J, Wang X, et al. Potential of large 'first generation' human-to-human transmission of 2019-nCoV[J] [published online ahead of print, 2020 Jan 30]. J Med Virol. doi:10.1002/jmv.25693.
[3] Rothe C, Schunk M, Sothmann P, et al. Transmission of 2019-nCoV Infection from an Asymptomatic Contact in Germany[J] [published online ahead of print,2020 Jan 30]. N Engl J Med, 2020. doi:10.1056/NEJMc2001468.[4] Lu R, Zhao X, Li J, et al. Genomic characterisation and epidemiology of 2019 novel coronavirus: implications for virus origins and receptor binding[J] [published online ahead of print, 2020 Jan 30]. Lancet, 2020.doi:10.1016/S0140-6736(20)30251-8.
[5] Zhou P, Yang XL, Wang XG, et al. A pneumonia outbreak associated with a new coronavirus of probable bat origin[J]. Nature, 2020. https://doi.org/10.1038/s41586-020-2012-7.
[6] Huang C, Wang Y, Li X, et al. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China. The Lancet. Published online January 24,2020. https://doi.org/10.1016/ S0140-6736(20)30183-5].
[7] Chen N, Zhou M, Dong X, et al. Epidemiological and clinical characteristics of 99 cases of 2019 novel coronavirus pneumonia in Wuhan, China: a descriptive study[J]. Lancet, 2020. https://doi.org/10.1016/S0140-6736(20)30211-7.
[8] Koren G, King S, Knowles S, et al. Ribavirin in the treatment of SARS: a new trick for an old drug? Canadian Medical Association or its licensors, 2003,168(10): 1289-1292.
[9] Momattin H, Mohammed K, Zumla A, et al. Therapeutic options for Middle East Respiratory Syndrome Coronavirus (MERS-CoV) – possible lessons from a 新型冠状病毒感染:医院药学工作指导与防控策略专家共识(第一版)28 systematic review of SARS-CoV therapy. International Journal of Infectious Disease, 2013, 17: e792-789.
[10] World Health Organization. Clinical management of severe acute respiratory infection when Novel coronavirus (2019-nCoV) infection is suspected: Interim Guidance. [EB/OL]. [2020-01-12]. https://www.who.int/docs/default-source/coronaviruse/clinical-management-of-novel-cov.pdf?sfvrsn=bc7da517_2.
[11] 中华人民共和国药典临床用药须知(中药成方制剂卷)2015年版.
[12] 刘松松, 谢益鸣. 101例藿香正气水药品不良反应文献分析[J].中国药物警戒,2017, 14(05): 317-320.
[13] 黄玲, 王艳, 吴曙粤. 中药麻黄药理作用研究进展[J].中外医疗, 2018, 37(07): 195-198.
[14] 白玉, 谭红. 连花清瘟胶囊致胃肠道不良反应1例[J]. 中国执业药师,2014,01: 47-48.
[15] 彭丽丽, 李岚, 沈璐, 李馨龄. 175例连花清瘟胶囊致药品不良反应/事件的文献分析[J]. 中国药物警戒, 2015, 12 (12): 753-755.
[16] 洪小凤, 林琴, 陈潇潇, 徐秀余. 血必净注射液不良反应影响因素的Logistic 回归分析[J]. 中国医院用药评价与分析, 2013, 13(10): 941-943.
[17] 贺定金, 瞿艳红. 60例参附注射液不良反应分析[J]. 中国药物警戒, 2014,11(03): 160-162.
[18] 赵茵, 邹丽, 王琳, 王泽华, 妊娠合并新型冠状病毒感染管理策略建议
[J/OL]. 华中科技大学协和医院. 线上发布.
[19] 王新燕, 吴杰, 鲁新华, 等. 河南省新型冠状病毒(2019-nCoV)感染孕产妇管理策略建议[J/OL]. 郑州大学学报(医学版): 1-3[2020-02-04]. https://doi.org/10.13705/j.issn.1671-6825.2020.01.167.
[20] Maxwell C, McGeer A, Tai KFY, et al. No. 225-Management Guidelines for Obstetric Patients and Neonates Born to Mothers with Suspected or Probable Severe Acute Respiratory Syndrome (SARS)[J]. J Obstet Gynaecol Can, 2017.39(8): e130-e137.新型冠状病毒感染:医院药学工作指导与防控策略专家共识(第一版)29
[21] 赵东赤,金润铭,刘智胜,尹薇. 湖北省儿童新型冠状病毒感染诊疗建议(试行第一版)[J]. 中国当代儿科杂志, 22(2): 96-99.
[22] 武汉大学中南医院新型冠状病毒感染的肺炎防治课题组,中国医疗保健国际交流会循证医学分会.新型冠状病毒(2019-nCoV)感染的肺炎诊疗快速建议指南(标准版).解放军医学杂志, 45(1): 1-20.
[23] Baiu I, Spain DA. Enteral Nutrition[J]. JAMA, 2019, 321(20):2040.doi:10.1001/jama.2019.4407.
[24] Baiu I, Spain DA. Parenteral Nutrition[J]. JAMA, 2019, 321(21):2142. doi:10.1001/jama.2019.4410.
[25] McClave SM, et al. Guidelines for the provision and assessment of nutrition support therapy in the adult critically ill patient: Society of Critical Care Medicine (SCCM) and American Society for Parenteral and Enteral Nutrition (A.S.P.E.N.). JPEN J Parenter Enteral Nutr. 2016; 40(2):159–211.
[26] Mueller CM, ed. The ASPEN Adult Nutrition Support Core Curriculum, 3rd Ed. Silver Spring, MD: ASPEN; 2017.
[27] 北京大学第三医院. 2019新型冠状病毒感染的肺炎药剂科管理工作应急预案(第四版)[J/OL]. [2020-02-01].
[28] 国家卫生健康委员会. 关于印发医疗机构内新型冠状病毒感染预防与控制技术指南(第一版)的通知[EB/OL]. [[2020-01-23]. http://www.nhc.gov.cn/xcs/yqfkdt/202001/b91fdab7c304431eb082d67847d27e 14.shtml.
[29] 中国心理卫生协会. 新型冠状病毒感染的肺炎公众心理自助与疏导指南[M].北京:人民卫生出版社, 2020.
[30] 国家卫生健康委疾控制局. 新型冠状病毒感染的肺炎疫情紧急心理危机干预指导原则[EB/OL]. [2020-02-06]. http://www.nhc.gov.cn/jkj/s3577/202001/6adc08b966594253b2b791be5c3b9467.shtml
.[31] 国家卫生健康委员会. 新型冠状病毒感染的肺炎防控中常见医用防护用品使用范围指引(试行)[EB/OL]. [2020-01-27]. http://www.nhc.gov.cn/xcs/zhengcwj/202001/e71c5de925a64eafbe1ce790debab 新型冠状病毒感染:医院药学工作指导与防控策略专家共识(第一版)305c6.shtml.
[32] 李舍予, 黄文治, 廖雪莲, 等. 新型冠状病毒感染医院内防控的华西紧急推荐[J]. 中国循证医学杂志, 2020, 20(3): 1-7.
[33] 原国家卫生部. 医疗卫生机构消毒技术规范(WS/T 367-2012)[EB/OL].2020-04-05.
[34] Rabenau HF, Cinatl J, Morgenstern B, et al. Stability and inactivation of SARS coronavirus[J]. Med Microbiol Immunol, 2005, 194(1-2): 1-6.
[35] Kim JY, Song JY, Yoon YK, et al. Middle east respiratory syndrome infection control and prevention guideline for healthcare facilities[J]. Infect Chemother,2015, 47(4): 278-302.
[36] 国家卫生健康委员会, 国家中医药管理局. 新型冠状病毒感染的肺炎防控方案(第三版) [EB/OL]. [2020-01-28]. http://www.nhc.gov.cn/jkj/s7923/202001/470b128513fe46f086d79667db9f76a5/files/8faa1b85841f42e8a0febbea3d8b9cb2.pdf..
[37] 国家卫生健康委员会办公厅. 关于进一步加强医疗机构感染预防与控制工作的通知[EB/OL]. [2019-5-18]. http://www.nhc.gov.cn/yzygj/s7659/201905/d831719a5ebf450f991ce47baf944829.shtml.
[38] 国家卫生健康委办公厅. 关于做好新型冠状病毒感染的肺炎疫情期间医疗机构医疗废物管理工作的通知[EB/OL]. [2020-1-28]. http://www.gov.cn/zhengce/zhengceku/2020-01/28/content_5472796.htm.
[39] 北京市卫生健康委员会. 医务人员(传染)感染性疾病隔离防护技术指南[EB/OL]. [2018-8-30]/[2020-2-3]. http://wjw.beijing.gov.cn/zwgk_20040/fgwj/bz/201912/t20191216_1239865.html.
[40] 北京市药学质量控制与改进中心. 关于医疗机构药学部门应对新型冠状病毒感染的肺炎的工作建议[EB/OL]. [2020-01-31]. http://www.nhc.gov.cn/yzygj/s7653p/202001/4294563ed35b43209b31739bd0785e67.shtml.新型冠状病毒感染:医院药学工作指导与防控策略专家共识(第一版)31
[41] 国家卫生健康委员会,国家中医药管理局. 《国家基本药物目录(2018年版)》[EB/OL]. [2018-09-30]. http://www.nhc.gov.cn/ewebeditor/uploadfile/2018/10/20181025183346942.pdf
[42] Holshue ML, DeBolt C, Lindquist S, et al. First Case of 2019 Novel Coronavirus in the United States[J]. N Engl J Med, 2020. DOI: 10.1056/NEJMoa2001191.
[43] 中华人民共和国国家卫生和计划生育委员会, 中华人民共和国国家中医药管理局. 卫生计生单位接受公益事业捐赠管理办法(试行)[J]. 中国实用乡村医生杂志, 2015, 22(23): 1-4.
[44] 国家食品药品监督管理总局.《药物临床试验质量管理规范》(局令第3号)[EB/OL]. [2003-08-06]. http://samr.sfda.gov.cn/WS01/CL0053/24473.html.
[45] 国家中医药管理局总后勤部卫生部. 医疗机构药事管理规定(卫医政发〔2011〕11号)[EB/OL]. 2011-03-01. http://www.satcm.gov.cn/fajiansi/gongzuodongtai/2018-03-24/2269.html.
致谢:
共识起草编写单位:北京大学第三医院、中国药学会医院药学专业委员会
主要编写人员(北京大学第三医院):
赵荣生、杨毅恒、杨丽、李子健、刘芳、任振宇、刘维、易湛苗、应颖秋、李潇潇、闫盈盈、李慧博、董淑杰、石伟龙、徐晓涵、周鹏翔、宋再伟、郑思骞、刘颖、周燊
共识专家:
翟所迪,北京大学第三医院
王育琴,首都医科大学宣武医院
朱 珠,北京协和医院
张 玉,华中科技大学同济医学院附属协和医院
梅 丹,北京协和医院
陈 孝,中山大学附属第一医院
武新安,兰州大学第一医院
缪丽燕,苏州大学附属第一医院
张毕奎,中南大学湘雅二医院
童荣生,四川省人民医院
李国辉,中国医科院肿瘤医院
敖海莲,和睦家医疗集团
史 琛,华中科技大学同济医学院附属协和医院
赵荣生,北京大学第三医院
(环球医学编辑:贾朝娟)
免责声明
版权所有©中国药学会。 本内容由环球医学整理,其观点并不反映优医迈或默沙东观点,此服务由优医迈与环球医学共同提供。
如需转载,请前往用户反馈页面提交说明:https://www.uemeds.cn/personal/feedback
新型冠状病毒感染:医院药学工作指导与防控策略专家共识(第一版)






 Copyright © 2025 Merck & Co., Inc., Rahway, NJ, USA and its affiliates. All rights reserved.
Copyright © 2025 Merck & Co., Inc., Rahway, NJ, USA and its affiliates. All rights reserved.