重症感染从狭义上说是指感染的重症状态,从广义上说还包括重症患者获得的感染。前者是重症医学诊治的重要疾病范畴,后者常在重症医学及其相关学科病房中发生。感染的重症状态可以一开始就发生,也可以是由轻到重地渐进发生。
感染是什么?是病原微生物入侵到患者体内的从局部播散到全身的一个过程。入侵过程中,微生物诱发患者的免疫反应过程,可以表现为免疫防御、免疫失控、免疫麻痹。而后两者又导致器官损伤、机体失调,进而患者因器官衰竭而死亡。
一、重症感染与感染的区别
在重症医学界,sepsis(脓毒症)是常用于描述感染的重症状态。sepsis这个词本身来自古希腊语,原意是指腐烂,相当于英文decay。希波克拉底认为sepsis是指组织破溃引起全身疾病、恶臭而最终死亡的这一过程。《第3版脓毒症与感染性休克定义国际共识》(The Third International Consensus Definitions for Sepsis and Septic Shock)工作组定义sepsis为:机体因感染应对失调而出现的危及生命的器官功能障碍。这个概念中指出:sepsis是器官功能障碍,而且是处在危及生命的状态,而感染只是触发的因素。sepsis是指重症到危及生命的感染状态,简言之即为重症感染。重症感染虽然源于感染,却不等同于感染。某些感染一发生就直接危及生命,有些虽然是同一类型病原微生物的感染但确有不同的临床过程。2008年,手足口病在暴发流行时,多数患儿仅表现为局灶性症状如发热、手心脚心出疹,但不发生器官衰竭,5~7天自愈。但一小部分患儿会突然出现急性肺水肿、弥漫性肺泡出血、急性脑水肿、颅内高压,甚至发生脑疝。可见即便是同样一种病毒感染也会发生不同的临床结局,那么为什么会出现上述现象呢?
二、重症感染的发生机制
1.病原微生物毒力
首先要说到的是病原微生物的毒力。20世纪80年代,我国台湾地区报道一组社区获得性肺炎克雷伯菌感染,可导致免疫正常的健康年轻人出现危及生命的感染,临床表现为肝脓肿、肺脓肿、脓胸、脑膜炎和眼内炎,并可以转移性播散。与普通的肺炎克雷伯菌相比,该菌更容易捕获铁离子产生荚膜,而生成高荚膜毒力的表型。
金黄色葡萄球菌也是一种高毒力菌,它可产生多糖荚膜并表达生成一系列毒力因子如杀白细胞素、α溶血素、苯酚溶解素、精氨酸分解素结合组织、分解组织,并可以结合血液中的免疫蛋白,实现免疫逃逸;同时可以分泌一系列细胞外酶,如蛋白酶、透明质酸酶、脂肪酶和核酸酶,这些酶有助于细菌破坏组织加快自身扩散,破坏膜的毒素还会对宿主细胞造成细胞溶解效应和组织损伤,成为导致感染性休克症状的超抗原。
志贺大肠埃希菌(VTEC)可以产生一种或多种噬菌体编码的志贺毒素,进入血液循环后造成血管内皮损伤并与微血管内皮细胞的受体结合,造成血小板活化和血栓形成;同时抑制血管性血友病因子(von Willebrand factor,vWF)剪切酶 ADAMTS13活性,导致形成超大分子的vWF异常释放,更容易结合血小板受体,促进微血管内血栓形成;甚至在VTEC感染使用抗菌药物治疗时,细菌裂解会使志贺毒素释放,造成更为严重的血管内凝血。
2.不适当的患者免疫反应及免疫调控
面临微生物入侵时,多数患者不发展成为重症感染的原因是恰当的免疫状态和免疫反应。机体免疫系统包括体液免疫、细胞免疫和神经调节机制等。微生物侵入人体时,免疫细胞通过模式识别受体如Toll样受体、C型凝集素受体、维甲酸诱导型基因1样受体和核苷酸结合寡聚化结构域样受体等,识别病原所特有的病原相关分子模式,受体会标示捕获这些异体蛋白,形成炎症小体,直接激活中性粒细胞、释放补体和启动凝血,诱导细胞的炎性坏死即焦亡(pyroptosis),细胞死亡所释放的内源性分子启动损伤相关分子模式(damage associated molecular pattern,DAMP),与模式识别受体结合上调炎症基因的转录并产生报警素(alarmins)启动强化上述炎症反应。同时感染导致的低血压、低灌注导致血管内皮损伤,导致跨膜糖蛋白的组织因子的暴露,后者作为Ⅶ因子受体激活凝血途径,并激活蛋白C和抗凝血酶,还产生Ⅰ型纤溶酶原抑制剂(plasminogen activator inhibitor,PAI)-Ⅰ抑制纤溶酶活化,促进凝血,发生重症感染性凝血病。
很多经过最初的重症感染打击后的患者会出现免疫抑制,表现为髓细胞上HLA-DR的表达减少。即使给予积极的抗感染治疗,这些患者的病灶迁延难以根除。许多研究表明,重症感染时血白细胞对病原微生物的敏感性下降,尸检资料也证实病死于重症感染患者的肺和脾功能严重受损。两者的间质细胞中T细胞抑制受体表达都增强了。这些现象表明机体除上述促进炎症的致炎反应外,还有调控炎症反应的抗炎反应。巨噬细胞可以表达为抗炎表型,与调节T细胞和髓源性抑制细胞一起减轻炎症反应,促使组织修复。除此之外还有神经炎症调节反射机制,炎症反应被感知后通过传入迷走神经传递到脑干,从脑干发出的传出迷走神经激活腹腔神经丛中的脾神经,导致脾脏中的去甲肾上腺素释放和CD4+T细胞亚群的乙酰胆碱分泌。乙酰胆碱释放结合巨噬细胞上的α7胆碱能受体,抑制促炎细胞因子的释放。在动物模型中,迷走神经切断更容易发生感染性休克,而刺激传出迷走神经或α7胆碱能受体减弱了全身炎症反应。
3.屏障功能破坏
人体通过皮肤和呼吸道、肠道、泌尿生殖道黏膜等天然的屏障将自然界异体物质与人体自身细胞相隔离,同时防止病原入侵。皮肤屏障包括物理性屏障、色素屏障、神经屏障、免疫屏障等;而肠屏障包括黏膜上皮、肠黏液、肠道菌群、分泌性免疫球蛋白、肠道相关淋巴组织、胆盐、激素和胃酸等。然而上述屏障会在疾病自身发展和接受治疗过程中受到损伤。严重创伤、烧伤、休克、大手术、炎性疾病、药物、毒物等因素可能直接损伤破坏皮肤和黏膜屏障导致病原微生物入侵,而治疗上述疾病时不可避免地会使用各种有创操作如静脉置管、气管插管、导尿管、鼻胃管、引流管,又会直接连通外界环境中的物质与人体内环境物质,使之成为病原微生物的入侵途径。
除了天然屏障外,还有人体免疫屏障功能的损伤。在许多长期慢性疾病未得到缓解的状态下,或者服用激素免疫抑制治疗,或者因为肿瘤进行放疗、化疗等情况下,抑制体液免疫和细胞免疫导致病原微生物更容易入侵。
4.感染初期的诊疗不及时
某些疾病状态下感染最初的临床特征不典型,与胰腺炎、创伤、大型外科手术等导致的炎症反应难以鉴别,而未被发现;某些感染灶部位隐匿,如颅内、腹膜后或实质器官内,导致原发病灶或未被及时发现,或未被早期引流根除;某些病原菌由于先前抗菌药物暴露出现耐药性,或者患者遭受罕见致病微生物感染,导致初始抗菌药物选择不适当;在感染初期未评估器官功能未及时进行器官保护,上述等情况的发生将导致病情加重。
三、重症感染的流行病学
在美国,重症感染约占住院患者的2%,是最常见的死亡原因,导致美国医保系统每年200亿美元的花费。这些患者中,一半以上(约75万例)收入重症监护病房(intensive care unit,ICU)进行治疗,约占重症医学科住院患者的10%。世界范围内每年大约有1 900万例重症感染患者。年龄、性别、种族都可能是重症感染的影响因素。婴儿和老人高发,男性比女性高发。发生重症感染的基因多态性近年来得到广泛研究。
重症感染患者部分发生在院外,部分发生在院内。其中肺炎约占一半,是最常见的病因;其次是腹腔感染和泌尿系感染。重症感染患者的血培养阳性率较低,不足三分之一。从一项全球75个国家14 000家重症医学科的资料中显示,革兰氏阴性菌约占分离菌的62%,革兰氏阳性菌约占47%,真菌约占19%。革兰氏阳性菌中金黄色葡萄球菌和肺炎链球菌是常见的分离菌,而在革兰氏阴性菌中大肠埃希菌、肺炎克雷伯菌属、铜绿假单胞菌是主要的分离菌。而耐药菌感染如不动杆菌、铜绿假单胞菌、真菌、耐药阳性球菌等会导致更长的住院时间和更高的死亡率。
四、重症感染的诊断
2016年《第3版脓毒症与感染性休克定义国际共识》工作组提出了脓毒症的新定义(即Sepsis 3.0),指出脓毒症是感染导致宿主免疫失衡进而引起致死性器官功能损伤的综合征。Sepsis 1.0中曾提出全身炎症反应综合征(systemic inflammatory response syndrome,SIRS)的概念,并认为 SIRS 是导致多器官功能不全(multiple organ dysfunction,MODF)最主要的原因。SIRS的诊断标准是具有以下4种表现中的任意2种或以上:①体温>38℃或<36℃;②心率>90次/min;③呼吸>20次/min或过度通气,PaCO2<32mmhg(1mmhg=0.133kpa);④血白细胞计数>12×109/L或血白细胞计数<4×109>10%。然而,人们在临床中逐步发现,SIRS敏感性高而特异性较差。任何一个轻微的感染甚至非感染因素(如剧烈运动)都有可能满足SIRS诊断标准,这与器官损伤及患者预后之间相关性较差。而脓毒症真正描述的是危及患者生命的器官功能障碍的感染,即重症感染。因此,该工作组将能更好反映器官功能障碍的序贯器官衰竭评估(sequential organ failure assessment,SOFA)替代SIRS纳入诊断标准中。SOFA评分是对呼吸、循环、肝脏、肾脏、凝血及神经系统等六大器官系统功能进行量化评分的一项标准,得分越高,器官功能越差。临床存在或者怀疑感染的患者,若其SOFA评分增加到≥2分则可以诊断为重症感染。在其后的验证实验中也证实SOFA评分在预测患者住院死亡率上要远远优于SIRS标准。其预测效率与多器官功能障碍逻辑性评价体系(logistic organ dysfunction score,LODS)的评分相近,但比LODS更便于临床操作执行。
在重症监护病房以外其他学科,SOFA评分并不是常规使用,上述工作组又根据重症患者的多个特征归纳出具有诊断意义的3个指标:①呼吸频率≥22次/min;②收缩压≤100mmHg;③神志的突然改变。具有上述任何两点或以上就提示存在重症感染的可能,这个简便的判定标准被称为快速SOFA(qSOFA)。《第3版脓毒症与感染性休克定义国际共识》提出并证实,在重症病房内使用SOFA评分预测患者死亡率的准确性要优于qSOFA,但在重症病房以外的其他科室使用qSOFA进行诊断的准确率要优于SOFA,而且qSOFA在操作上也十分方便,所以推荐在重症病房以外的其他科室怀疑重症感染时,可以先使用qSOFA进行评分,若得分≥2分则需要密切监视此类患者并对其进行SOFA评分,若SOFA得分较基线水平增加2分及以上,则可认为患者存在器官功能损害,可以诊断为重症感染。
重症感染时常常会导致患者血流动力学紊乱,造成组织灌注不足、高乳酸血症,此时称为感染性休克(septic shock)。感染性休克是重症感染的亚型,具有高达40%的患者病死率。它更强调由于感染导致的血流动力学紊乱,进而造成的低血压或组织低灌注状态,此时即便是经过充分液体复苏治疗,也仍然需要应用血管活性药物才能维持平均动脉压(MAP)≥65mmHg,同时血乳酸水平>2mmol/L。重症感染和感染性休克诊断流程见图1。
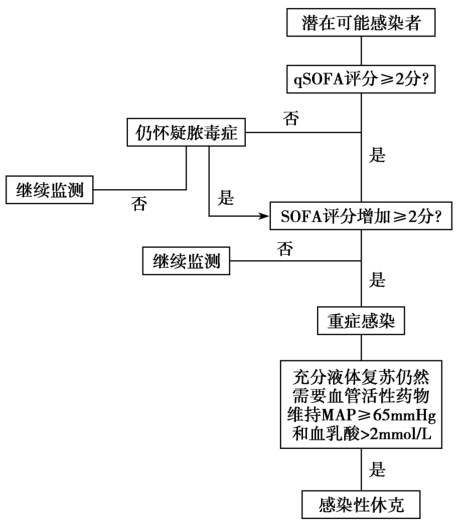
图1 重症感染和感染性休克诊断流程
qSOFA:快速 SOFA;MAP:平均动脉压
五、重症感染的筛查及早期识别
与急性心肌梗死一样,早期识别重症感染是治疗重症感染的关键。研究报道,在重症感染发生后,每延误一个小时的治疗都可能导致死亡率显著升高,而早期发现后即刻输入抗菌药物和液体治疗改善这类患者的预后。然而困难的是,重症感染早期的表现有可能是隐匿而不特异的,尤其对于目前的临床管理体系而言,临床上对重症感染的早期识别及启动治疗变得困难。
重症感染的筛查首先要从临床一线医护人员做起。筛查阳性包括临床诊断感染和发现器官功能障碍两个部分组成。临床诊断感染需要熟练掌握对不同部位感染的诊断标准,然而更为重要的是及时发现器官功能障碍。与早期预警评分(NEWS)、SIRS评分和qSOFA评分等床旁易评估指标不一样的是,SOFA评分更依赖于血气、血常规、肝肾功能等实验室检查。在临床实践中重点培训临床一线医护人员熟练掌握SOFA的指标,及时进行检测尽快获取上述数据,以增加筛查准确性和敏感性。有一项研究中以护理为导向实行为期1个月的重症感染筛查,护士们在每天每班开始前两小时对每位患者进行筛查,结果发现245例患者中39例阳性,改变了40%~50%上述患者的临床医疗行为,如使用抗菌药物、留取血培养、液体复苏、检测乳酸和转入重症医学科等。通过这些活动,促进护理人员对筛查的理解,培训更多人员成为院内重症感染识别的专家,而且改进了工作流程,并且更为重要的是改善了患者的预后。研究发现在一家医院中严格执行标准化的筛查,将每天至少多挽救1位患者的生命。
值得注意的是,当前国内外都在实施医疗病历电子信息系统,可在同一时间收集患者所有的包括床旁生命体征及实验室检查的所有医疗信息,尤其是对于相对重症的患者会有持续的监护,这样连续的监测信息被实时记录下来。而人们也在尝试将这些信息进行分析整合做出电子诊断以早期发现重症感染患者,进行电子预警,而且可以启动诊断后的集束化治疗即临床决策系统。这样电子预警结合临床决策可以将重症感染的诊断和起始治疗的时间明显提前。
当然如何优化这些诊断的敏感性和特异性也是重要问题。其中最为重要的是如何确定重症感染起始的零点。绝对的零点对于急诊患者而言,在于诊室进行分诊的即刻。而对于住院患者而言,零点的发现更有意义,临床医师早期发现零点拥有更多改善患者预后的机会。
根据《第3版脓毒症与感染性休克定义国际共识》诊断依据,电子信息系统感知感染的诊断是指同时采集到临床应用抗菌药物及其前72小时或后24小时进行微生物送检的信息。而重症感染的诊断是在诊断感染的同时满足序贯器官衰竭评估(SOFA)比基础值增加两分及以上。临床操作中可以首先获取SOFA变化的时间点,同时确认此时是否满足感染的诊断,如满足此时SOFA变化时间点即为感染的零点。
人工智能技术的引入使得重症感染的发现更为提前。有研究对数以万计的重症患者的临床资料进行学习,每小时获取65个指标,进行演算推导感染发生的零点,从而建立诊断重症感染模型,并通过在更大的数据库中进行验证,最终使得重症感染的诊断提前4~12小时。
六、重症感染的治疗措施
重症感染时各器官进行性出现损伤甚至衰竭,可谓生命垂危、命悬一线。其拯救治疗涵盖早期液体复苏、抗菌药物使用、机械通气、激素应用、血糖控制和肠内营养等多个方面。治疗需要精确性,需要涉及学科发展的前沿领域,需要统一标准,才能最大限度地抢救上述患者的生命。从2004年开始,世界多个重症医学组织每4年联合发布一次拯救重症感染的指南,其内容提出一系列快速、密集、捆绑式治疗策略,几乎涵盖重症感染治疗的所有领域。该指南是以循证医学为依据,根据最新重症医学领域临床研究进展,采用Grade分级进行证据分级,提出推荐意见。其中2016年“拯救脓毒症战役”(Surviving Sepsis Campaign,SSC)指南包括来自25个国际重症感染组织的55名专家从655篇参考文献中提出的93条推荐意见,其中32条为强烈推荐、39条为弱推荐,18条为最佳临床实践推荐、4条未形成推荐意见。内容涉及液体复苏、感染筛查、血管活性药物应用、初始抗菌药物治疗、机械通气、营养等21个领域。其推荐意见字斟句酌,具有显著的循证医学特征。
同时重症感染的治疗既要准确,更要速度。从某种程度上说,治疗是与时间赛跑的过程。2008年SSC指南曾提出6小时集束化复苏策略,包括应用血管加压药将平均动脉压(MAP)维持在≥65mmHg;初始复苏后仍持续低血压或者初始乳酸为≥4mmol/L的情况下;测量中心静脉压(CVP)及中心静脉血氧饱和度(SCVO2);如果初始乳酸升高,则需要复测乳酸;其中提出4个6小时液体复苏需达到的目标,即CVP约12mmHg、MAP≥65mmHg、SCVO2≥70%、尿量≥0.5ml/(kg·h)。 在 2012 年SSC指南又提出3小时集束化复苏策略,即测量乳酸水平,在使用抗菌药物之前获得血培养标本,应用广谱抗菌药物,对于低血压或乳酸≥4mmol/L的患者,应用30ml/kg的晶体液进行液体复苏。在2018年SSC指南甚至提出1小时集束化复苏策略,测量乳酸,如果初始乳酸高,再重复测量,应用抗菌药物前留取血培养,起始抗菌药物治疗,仍持续低血压或者初始乳酸为≥4mmol/L的情况下起始30ml/kg的快速晶体液复苏,充分液体复苏后应用血管活性药物维持血压在65mmHg以上。虽然上述推荐意见仍存在争论,但能看出对重症感染治疗的特征,其一具有时间紧迫性,集束化目标由6小时到3小时再到1小时,其二治疗具有目标性,包括血乳酸、MAP、血培养、抗菌药物、足量的液体等。
重症感染这个看似很古老的疾病却由于每年导致大量的患者死亡,一直是临床医学最为紧迫的话题。近年来,随着重症医学的快速发展及循证医学的传播,越来越多的重症感染患者得到及时准确的救治而存活下来。然而,诊断和治疗的规范远远未普及,更多的临床及研究的热点问题逐渐浮现,越来越多的临床医师和研究者正投入重症感染领域中,其中不乏来自国内的声音,一场崭新战役的号角已悄然吹起。
(隆 云)
免责声明
版权所有©人民卫生出版社有限公司。 本内容由人民卫生出版社审定并提供,其观点并不反映优医迈或默沙东观点,此服务由优医迈与环球医学资讯授权共同提供。
如需转载,请前往用户反馈页面提交说明:https://www.uemeds.cn/personal/feedback
1.IDSA Sepsis Task Force.Infectious Diseases Society of America(IDSA)Position Statement:Why IDSA Did Not Endorse the Surviving Sepsis Campaign Guidelines[J].Clin Infect Dis,2018,66:1631-1635.
2.KLEIN KLOUWENBERG PM,CREMER OL,VAN VUGHT LA,et al.Likelihood of infection in patients with presumed sepsis at the time of intensive care unit admission:a cohort study[J].Crit Care,2015,19:319.
3.SINGER M,DEUTSCHMAN CS,SEYMOUR CW,et al.The Third International Consensus Definitions for Sepsis and Septic Shock(Sepsis-3)[J].JAMA,2016,315:801-810.
4.RHODES A,EVANS LE,ALHAZZANI W,et al.Surviving Sepsis Campaign:International Guidelines for Management of Sepsis and Septic Shock:2016[J].Crit Care Med,2017,43:486-552.
5.GOULDEN R,HOYLE MC,MONIS J,et al.qSOFA,SIRS and NEWS for Predicting Inhospital Mortality and ICU Admission in Emergency Admissions Treated as Sepsis[J].Emerg Med J,2018,35:345-349.
6.GYANG E,SHIEH L,FORSEY L,et al.A nurse-driven screening tool for the early identification of sepsis in an intermediate care unit setting[J].J Hosp Med,2015,10:97-103.
7.JONES SL,ASHTON CM,KIEHNE L,et al.Reductions in sepsis mortality and costs after design and implementation of a nurse-based early recognition and response program[J].Jt Comm J Qual Patient Saf,2015,41:483-491.
8.LEVY MM,RHODES A,PHILLIPS GS,et al.Surviving Sepsis Campaign:association between performance metrics and outcomes in a 7.5-year study[J].Crit Care Med,2015,43:3-12.
9.ANDES DR,SAFDAR N,BADDLEY JW,et al.Impact of treatment strategy on outcomes in patients with candidemia and other forms of invasive candidiasis:a patient-level quantitative review of randomized trials[J].Clin Infect Dis,2012,54:1110-1122.
10.BRUNIHORST FM,OPPERT M,MARX G,et al.Effect of empirical treatment with moxifloxacin and meropenem vs meropenem on sepsis-related organ dysfunction in patients with severe sepsis:a randomized trial[J].JAMA,2012,307:2390-2399.
11.DE JONG E,VAN OERS JA,BEISHUIZEN A,et al.Efficacy and safety of procalcitonin guidance inreducing the duration of antibiotic treatment in critically ill patients:a randomised,controlled,open-label trial[J].Lancet Infect Dis,2016,16:819-827.
12.PRKNO A,WACKER C,BRUNKHORST FM,et al.Procalcitoninguided therapy in intensive care unit patients with severe sepsis and septic shock—a systematic review and metaanalysis[J].Crit Care,2013,17:R291.
13.BLOT SI,PEA F,LIPMAN J.The effect of pathophysiology on pharmacokinetics in the critically ill patient—concepts appraised by the example of antimicrobial agents[J].Adv Drug Deliv Rev,2014,77:3-11.
14.AVNI T,LEVCOVICH A,AD-E DD,et al.Prophylactic antibiotics for burns patients:systematic review and meta-analysis[J].BMJ,2010,340:c241.
15.BARAJAS-NAVA LA,LOPEZ-ALCALDE J,ROQUI FIGULS M,et al.Antibiotic prophylaxis for preventing burn wound infection[J].Cochrane Database Syst Rev,2013,6:CD008738.
16.SAWYER RG,CLARIDGE JA,NATHENS AB,et al.Trial of shortcourse antimicrobial therapy for intraabdominal infection[J].N Engl J Med,2015,372:1996-2005.
17.ELIAKIM-RAZ N,YAHAV D,PAUL M,et al.Duration of antibiotic treatment for acute pyelonephritis and septic urinary tract infection-7 days or less versus longer treatment:systematic re-view and meta-analysis of randomized controlled trials[J].J Antimicrob Chemother,2013,68:2183-2191.
18.RATTAN R,ALLEN CJ,SAWYER RG,et al.Patients with complicated intra-abdominal infection presenting with sepsis do not require longer duration of antimicrobial therapy[J].J Am Coll Surg,2016,222:440-446.
19.SEYMOUR CW,LIU VX,IWASHYNA TJ,et al.Assessment of Clinical Criteria for Sepsis:For the Third International Consensus Definitions for Sepsis and Septic Shock(Sepsis-3)[J].JAMA,2016,315:762-774.
20.SHANKAR-HARI M,PHILLIPS GS,LEVY ML,et al.Developing a New Definition and Assessing New Clinical Criteria for Septic Shock:For the Third International Consensus Definitions for Sepsis and Septic Shock(Sepsis-3)[J].JAMA,2016,315:775-787.
人卫知识数字服务体系






 Copyright © 2025 Merck & Co., Inc., Rahway, NJ, USA and its affiliates. All rights reserved.
Copyright © 2025 Merck & Co., Inc., Rahway, NJ, USA and its affiliates. All rights reserved.
